Mortalitätsrisiko bei COPD – Faktoren und Gegenmaßnahmen
Interessengebiete: Allgemeinmedizin und Innere Medizin, Geriatrie, Pneumologie
Die chronisch obstruktive Lungenerkrankung (COPD) ist durch eine Abwärtsspirale gekennzeichnet: Die Lungenfunktion verschlechtert sich, die Exazerbationen nehmen zu,
die Hospitalisierungsraten häufen sich und das Mortalitätsrisiko ist hoch. Die COPD-Mortalität wird vor allem vom Lebensalters, dem Gewichtsverlust sowie von Komorbiditäten wie Lungenkrebs und kardiovaskulären Erkrankungen beeinflusst. Aktuelle Leitlinien empfehlen medikamentöse und nichtmedikamentöse Maßnahmen zu kombinieren, um Exazerbationen zu verhindern. Pharmakologische Studien wie IMPACT und ETHOS heben die Bedeutung von inhalativen Kortikosteroiden in Form einer Triple-Therapie bei häufigen Exazerbationen hervor.
Kursinhalt
Die chronisch obstruktive Lungenerkrankung (COPD) ist durch eine Abwärtsspirale gekennzeichnet: Die Lungenfunktion verschlechtert sich, die Exazerbationen nehmen zu, die Hospitalisierungsraten häufen sich und das Mortalitätsrisiko ist hoch. Die COPD-Mortalität wird vor allem vom Lebensalters, dem Gewichtsverlust sowie von Komorbiditäten wie Lungenkrebs und kardiovaskulären Erkrankungen beeinflusst. Aktuelle Leitlinien empfehlen medikamentöse und nichtmedikamentöse Maßnahmen zu kombinieren, um Exazerbationen zu verhindern. Pharmakologische Studien wie IMPACT und ETHOS heben die Bedeutung von inhalativen Kortikosteroiden bei häufigen Exazerbationen hervor.
00:00:16
Liebe Kolleginnen und Kollegen. Ich begrüße Sie ganz herzlich zu unserer CME-Fortbildung zum Thema Mortalitätsrisiko bei COPD – Faktoren und Gegenmaßnahmen. Hier meine Interessenskonflikte, kurz dargestellt. Ich denke, COPD und Exazerbationen sind bei unseren Patientinnen und Patienten mit COPD ein sehr, sehr großes Thema und ein Problem. Ich denke, vor allem die Exazerbationen sind in den letzten Jahren deutlich in den Vordergrund getreten und deren Wichtigkeit haben wir verstanden. Ich stelle ein Beispiel eines Patienten mit COPD und Exazerbationen dar. Dieser Patient erhielt eine Kombination aus einem lang wirksamen Betamimetikum und einem lang wirksamen Anticholinergikum. Als Begleiterkrankung bestand bei ihm ein arterieller Hypertonus. Was waren die Symptome? Belastungsdyspnoe, er konnte kaum noch die Treppen steigen, und er hatte vor allem bei den hohen Temperaturen im Sommer Luftprobleme. Er hatte vor allem morgens produktiven Husten, wahrscheinlich aus der Nacht heraus. In den letzten zwölf Monaten hatte er zwei Exazerbationen, die jeweils ambulant mit einem Prednisolon-Stoß behandelt werden konnten. Das Differenzialblutbild, das vorlag, zeigte einen erhöhten Anteil von eosinophilen Granulozyten mit 300 pro Mikroliter. Das sind die Rahmenbedingungen.
00:01:38
Da stellen sich die Fragen, welche Faktoren müssen wir bei diesen Patientinnen und Patienten berücksichtigen? Worauf müssen wir schauen? Welche Maßnahmen müssen wir für die richtige Versorgung treffen? Das Wichtigste ist, wie arbeiten wir präventiv gegen diese Exazerbationen? Ich denke, das sind drei wichtige Fragen, denen wir uns heute widmen möchten.
00:02:02
Wenn wir uns die Einteilung der Exazerbationen nach der NVL anschauen, wird in leichte, mittelschwere, schwere und sehr schwere Exazerbationen unterschieden. Die leichten Exazerbationen sind aus meiner Sicht für uns Ärzte besonders schwierig zu erkennen. Warum? Der Patient führt eine Bedarfsmedikation durch und geht nicht zum Arzt. Das Schlimme ist, wenn er bei uns sitzt und wir ihn fragen, ist es häufig, dass er sich nicht mehr erinnern kann. Er hat sein Spray mehrfach und über einige Tage gebraucht und es ging ihm schlechter. Er hat es innerhalb des Intervalls vergessen, wenn es etwas länger her ist. Die mittelschweren Exazerbationen sind leichter zu erkennen. In diesem Fall verschreibt der Arzt ihm aufgrund seiner Beschwerden Medikamente. In der überwiegenden Anzahl ist dies ein Kortison- oder Prednisolon-Stoß. Wenn dazu eine bakterielle Superinfektion eine Rolle spielt, bekommt er zusätzlich ein Antibiotikum. Dabei ist wichtig, im Auge zu behalten, dass 70 bis 80 Prozent unserer Exazerbationen primär viral getriggert sind.
Bei der schweren Exazerbation muss der Patient stationär behandelt werden, aufgrund der Verschlechterung seines Allgemeinzustandes. Es kann sein, dass ihn der Notarzt dann am Wochenende mitgenommen hat, weil es ihm so schlecht ging. Die sehr schweren Exazerbationen sehen wir zum Glück nicht mehr häufig. Dem Patienten geht es so schlecht, dass er wegen starker Atemnot und vor allem wegen eines zusätzlichen Sauerstoffmangels primär auf eine Intensivstation muss.
00:03:50
Was ist problematisch bei unseren Exazerbationen? Wir haben gelernt, dass ein Patient, der häufig eine Exazerbation hat, immer wieder oder gehäuft eine bekommt. Sie sehen hier Daten einer großen Erhebung von über 73.000 Patientinnen und Patienten. Sie sehen, wenn bereits eine schwere Exazerbation war, steigt das Risiko für eine erneute schwere Exazerbation. Man sieht, dass die Zeitabstände zwischen diesen Exazerbationen immer kürzer werden. Das heißt, es ist wie ein Teufelskreis, der sich an dieser Stelle verstärkt.
00:04:27
Das zweite große Problem, das wir mit den Exazerbationen haben, ist, dass die Exazerbationen mit der Mortalität korrelieren. Das heißt, jede Exazerbation, auch die moderate, erhöht das Sterberisiko.
Das heißt, Exazerbationen zu vermeiden bedeutet, Mortalität zu reduzieren. Wir sehen, dass bei Patientinnen und Patienten, die mindestens eine schwere Exazerbation haben, 25 Prozent der COPD-Patientinnen und -Patienten nach drei Jahren verstorben waren. Das heißt, je häufiger, desto größer ist das Risiko für die Patientinnen und Patienten, dass das Ganze fatal endet. Das heißt, wir müssen Exazerbationen vermindern, verhindern. Im Endeffekt kann man sagen, die Exazerbation ist wie der kleine Herzinfarkt beim Kardiologen.
00:05:17
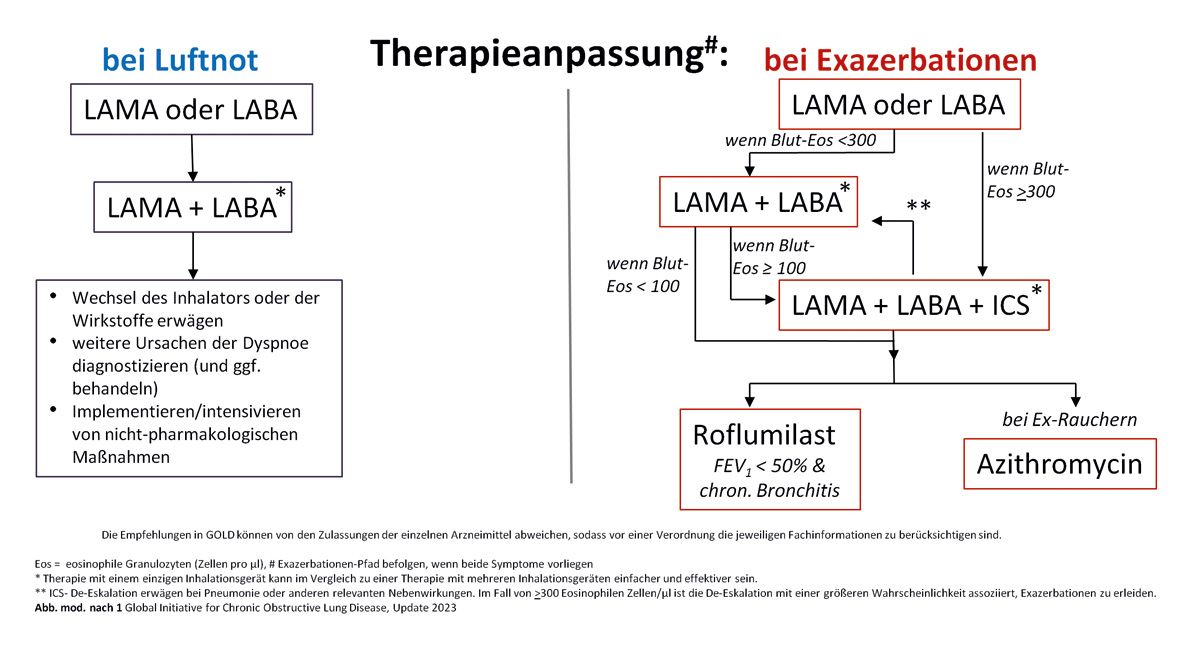
Wie sieht diese Behandlung dieser exazerbierten Patientinnen und Patienten aus? Was empfiehlt und sagt uns die Leitlinie? Bei der Leitlinie müssen wir zwischen der Nationalen Versorgungsleitlinie (NVL) und der GOLD-Empfehlung (Abb. 1) unterscheiden. NVL ist keine klassische Leitlinie, hat aber eine Empfehlung. Ich denke, dass unsere NVL sich nach den Standards von GOLD gerichtet hat und für Deutschland deutlich modifiziert wurde.
Da hat sich durchgesetzt, dass wir in der Therapieanpassung unterscheiden. Einmal haben wir Patientinnen und Patienten, bei denen vor allem die Luftnot im Vordergrund steht. Hier wird häufig entweder mit einem lang wirksamen Anticholinergikum oder mit einem lang wirksamen Bronchial-Dilatator, Betamimetikum in der Therapie begonnen. Wir haben gelernt, wenn das nicht ausreichend ist bei diesen Patientinnen und Patienten, kommen wir recht zügig zur dualen Bronchodilatation. Wenn keine zufriedenstellende Therapie da ist, ist es nicht wichtig, direkt eine Therapieeskalation durchzuführen. Es ist wichtig, dass man schaut, was die Ursachen für das Ganze sind. Liegt es am Inhalator? Kommt der Patient mit seinem Inhalator nicht zurecht? Wir sollten uns vom Patienten unbedingt zeigen lassen, dass er ihn richtig verwendet. Für die Luftnot sind Differenzialdiagnosen wichtig. Gibt es Begleiterkrankungen? Sind diese Begleiterkrankungen richtig diagnostiziert und werden sie richtig behandelt? Zusätzlich können wir nichtmedikamentöse Maßnahmen dazunehmen, wie Physiotherapie. Im Rahmen des DMPs ist Lungensport, zum Beispiel, als Stichwort sehr wichtig. Hier geben wir den Patientinnen und Patienten die Möglichkeit, sich zu konditionieren. Wir wirken so vor allem der negativen Abwärtsspirale, der fehlenden Belastbarkeit und der Verschlechterung der Gesamtsituation entgegen.
Das Ganze sieht etwas anders aus, wenn die Exazerbationen gehäuft sind beziehungsweise im Vordergrund stehen. Wenn wir mit einer Monotherapie kommen, gibt es verschiedene Bereiche. Sehen wir einen Patienten, der in der Absolutzahl einen höheren Anteil an Bluteosonophilen hat und Exazerbationen spielen eine Rolle, ist es wichtig, dass man im Rahmen einer Eskalation auf eine duale Bronchodilatation schnell ein inhalatives Steroid dazu nimmt. Sind die Eosinophilen nicht erhöht? Bei nicht ausreichender, alleiniger Monotherapie ist die duale Bronchodilatation die zentrale Therapieoption. Wir haben gelernt, wenn eine Exazerbation vorliegt oder die Eosinophilen erhöht sind und Exazerbationen im Vordergrund stehen, das inhalative Steroid schnell in die Therapie zu implementieren. Dadurch können wir Exazerbationen verhindern. Wenn die Eosinophilen deutlich erniedrigt sind oder zusammen mit Steroiden eine Pneunomie aufgetreten ist, sollte das Steroid nicht in die Therapie integriert werden. Eine weitere Option, die wir haben, ist das Roflumilast. Dieses spielt vor allem beim bronchitischem Typ eine große Rolle. Eine weitere Rolle spielt das Azithromycin, für das eine Off-Label-Therapie besteht und in der Form keine Zulassung vorliegt. Das sind Einzelfallentscheidungen bei Patientinnen und Patienten, die aus der Klinik kommen, bei denen aufgrund gehäufter Exazerbationen dieser Schritt gegangen wird.
Therapieanpassung bei Exazerbationen, wie ist es damit? Man sollte nicht lange warten. Die große Diskussion und Frage ist, wie viele Exazerbationen sollen stattfinden oder wie viele wollen wir abwarten, bis wir eine Therapieeskalation vornehmen? Das heißt, aus dem Alltag haben wir gelernt, dass jede Exazerbation eine zu viel ist. Spätestens nach der zweiten Exazerbation sollte das ICS, das inhalative Steroid, dazugenommen werden. Aus meiner Sicht ist es weiterhin sehr wichtig. Ich denke, da gibt es eine gute Zusammenarbeit mit den Hausärzten. Im Rahmen des großen Blutbilds schauen wir bei unseren Patientinnen und Patienten nach den Werten für die Eosinophilen.
Ist dieser Wert größer 300 ist das ein Zeichen und wir wissen, diese Patientinnen und Patienten neigen zu gehäuften Exazerbationen. Es sollte ein innovatives Steroid frühzeitig in die Therapie implementiert werden.
00:10:21
Ist es möglich, Exazerbationen und Mortalität zu reduzieren? Ich möchte Ihnen Daten zu Studien vorstellen, wie die medikamentöse Therapie einen Einfluss auf das Mortalitätsrisiko bei der COPD gezeigt hat. Bevor wir dazu kommen ist es wichtig, dass wir über Risikofaktoren für COPD und COPD-Mortalität sprechen. Wir fangen mit COPD an. Wir wissen, dass Rauchen einer der wichtigsten, größten Faktoren und Treiber ist. Man darf nicht vergessen, dass toxische Partikel, Gase und Umweltschadstoffe genauso eine Rolle spielen können. Wir wissen, dass ein erhöhter CO2-Partialdruck eine Rolle spielt. Wir wissen, dass mit einer COPD ein erhöhter Lungenhochdruck eine Rolle spielen kann, der durch die Schädigung der Lungenstrombahn zustande kommt. Wir wissen, die COPD-Mortalität wird vor allem von Faktoren beeinflusst wie die Höhe des Lebensalters sowie Gewichtsverlust, da ein sehr niedriger BMI ein negativer Prädiktor ist. Wir wissen, dass Komorbiditäten eine große Rolle spielen, der Lungenkrebs zum einen, aber auch die kardiovaskuläre Komorbidität. Ich denke, diese ist in letzter Zeit auch in der Interaktion mit der COPD deutlich in den Vordergrund getreten. Wir wissen, dass vormalige oder bereits stattgefundene Hospitalisierungen sich negativ auf die COPD-Exazerbationen auswirken. Wir sehen, diese Patientinnen und Patienten erleiden häufiger wieder eine. Wir wissen, dass durch das Ganze die Lebensqualität bei unseren Patientinnen und Patienten verschlechtert und negativ beeinflusst wird. Lassen Sie uns zu Mortalitätsdaten kommen.
Da muss man sagen, dass vor der IMPACT-Studie keine pharmakologische Therapie eine Reduktion des Mortalitätsrisikos bei COPD-Patientinnen und -Patienten in einer prospektiven klinischen Studie zeigen konnte. Es war in dieser Studie kein primärer oder sekundärer Endpunkt, jedoch war es in dieser Studie darstellbar. Wir hatten im Vorfeld einige Studien, die den Hinweis gaben, dass eine ICS-haltige Therapie das Mortalitätsrisiko bei COPD-Patientinnen und -Patienten senken könnte.
00:12:59
Die spannende Frage war, bietet eine ICS-haltige Triple-Therapie bei symptomatischen COPD-Patientinnen und -Patienten einen Überlebensvorteil? Schauen wir auf das Studiendesign der IMPACT-Studie. Es ist besonders hervorzuheben, dass wir zum ersten Mal eine Studie hatten, bei der Patientenzahlen eingeschlossen wurden, die uns an pathologische Studien erinnern. Wenn wir sonst schauten, waren wir als Pneumologinnen und Pneumologen stolz, wenn 2.000, 2.500 Patientinnen und Patienten eingeschlossen werden konnten. Hier waren es über 10.000 Patientinnen und Patienten in einer 52-Wochen-Studie. Der zweite Vorteil oder die zweite Besonderheit, die ich an der Stelle hervorheben wollte, was uns in anderen Studien Probleme gemacht hat, dass wir mit verschiedenen Inhalatoren gearbeitet hatten. Hier waren für alle Patientinnen und Patienten die gleichen Bedingungen, sprich ein gleicher Inhalator. In dieser Studie hatten wir drei Arme gehabt. Einmal eine Triple-Therapie, kombiniert mit einer Kombination aus einer dualen Bronchodilatation und als dritter Arm die Kombination aus einem inhalativen Steroid und einem lang wirksamen Betamimetikum. Ich denke, das ist eine spannende Geschichte. Die Frage war, wie sah das Ganze nach 52 Wochen aus? Es wurde danach geschaut. Schauen wir uns die Einschlusskriterien an: über 40, CAT größer 10, FEV1 unter 50 Prozent und eine moderate oder schwere Exazerbation im vergangenen Jahr. Ich denke, der zweite Punkt ist wichtig, weil es uns um Exazerbation ging. Der FEV1 konnte zwischen 50 und 80 Prozent sein, wenn 2 moderate oder 1 schwere Exazerbation im Jahr davor waren. Ausschlusskriterien waren aktuelle Asthma-Symptomatik, ein Alpha-1-Antitrypsin-Mangel oder andere Lungenerkrankungen. Es ist wichtig, dass erhöhte Bluteosinophilie kein Einschlusskriterium waren.
00:15:00
Wie war dieses Studiendesign? Wir haben primäre und sekundäre Endpunkte, wie Sie wissen. Der primäre Endpunkt oder die co-primären Endpunkte waren die jährliche Rate an moderaten und schweren Exazerbationen. Das ist das, was wir wollten. Wir haben in diesem Zusammenhang geschaut, wie stellt sich die Triple-Therapie gegen die beiden Arme der Zweifachtherapie? Sprich, wie stellt sich die duale Bronchodilatation beziehungsweise die Kombination aus inhalativem Steroid und lang wirksamen Betamimetikum dar? Sekundäre Endpunkte, auf die wir schauen, waren, wie sich die FEV1 ändert. Wie ändert sich die Lebensqualität? Wie ist die Zeit bis zur ersten moderaten, schweren Exazerbation? Wie ändert sich die Rate der schweren Exazerbationen bei Patientinnen und Patienten mit Hinblick auf eine Eosinophilen-Zahl über 150? Es spielten Subgruppenanalysen eine Rolle. Es war kein sekundärer, aber vordefinierter Endpunkt der Zeit, die Zeit bis zum Tod jeglicher Ursache und das On-/Off-Treatment. Warum ist es wichtig? Ein primärer Blick auf die Mortalität ist wichtig, weil uns die Daten aus anderen Analysen davor gefehlt haben.
00:16:30
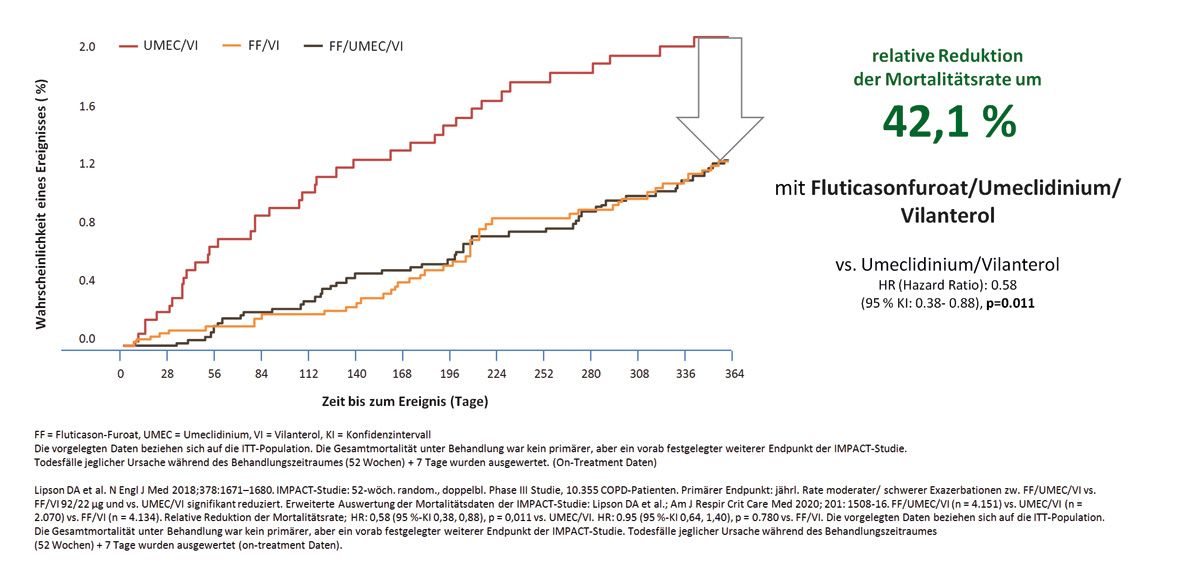
Hier sehen Sie das beeindruckende Ergebnis der IMPACT-Studie. Wir haben eine Triple-Therapie gegen eine duale Bronchodilatation verglichen. Sie sehen, dass es bei der Mortalitätsrate zu einer relativen Reduktion um 42,1 Prozent gekommen ist, wenn man eine Therapie mit einer dualen Bronchodilatation mit einer Triple-Therapie, wie hier dargestellt, vergleicht (Abb. 2). Ich denke, das ist ein sehr, sehr beeindruckendes Ergebnis, vor allem wenn man im Hinterkopf hat, dass in der FLAME-Studie der Stellenwert der dualen Bronchodilatation im Vergleich zu einer Kombination aus einem ICS und einem lang wirksamen Betamimetikum damals anders ausgesehen hat.
Schauen wir uns die Subgruppen im Vergleich an. Sie sehen an unseren Post-hoc-Analysen der IMPACT-Studie, dass es eine ausgewogene Situation hinsichtlich Geschlecht, Alter und der ethnischen Situation gab. Die Subgruppen waren weitestgehend konsistent. An dieser Stelle hat man hinsichtlich der Exazerbation weitergeschaut. Die kardiovaskulären Risiken wie Raucherstatus, BMI und Pneumonie-Historie traten als ein bedeutender Faktor auf. Es war zu sehen, dass es vor allem bei den Patientinnen und Patienten in den untersuchten Gruppen mit mehr als einem oder zwei Risikofaktoren zu einer Reduktion der Mortalitätsrate gekommen ist. Das heißt, das kardiovaskuläre Risiko stellte sich als ein Faktor da, bei dem man vor allem bei den Risikofaktoren genauer hinschauen konnte. Interessant war das Thema Pneumonie, es gab keine unerwarteten Ereignisse. Hinsichtlich der Pneunomien entsprach es den Ergebnissen, die wir im Vorfeld kannten und erwartet hatten.
00:18:44
Wir schauen genauer auf die Relevanz der eosinophilen Granulozyten. Wenn man in die Gruppe von unter 150 Eosinophilen und über 150 Eosinophilen unterteilt, wird deutlich, dass wir hinsichtlich der jährlichen Rate an moderaten und schweren Exazerbation für die entsprechende Triple-Therapie einen Vorteil sahen. In dem Fall war auffällig, dass, je höher die Eosinophilen waren, desto größer war der Vorteil der Triple-Therapie. Es war sehr interessant, dass vor allem in der Gruppe der Patientinnen und Patienten mit über 150 Eosinophilen, der Vorteil einer Kombinationstherapie aus einem inhalativen Steroid und einem lang wirksamen Betamimetikum im Vergleich zu einer dualen Bronchodilatation signifikant war.
An dieser Stelle war die Triple-Therapie deutlich besser. Hier schien das inhalative Steroid zu helfen, die Exazerbationsrate zu senken. Das heißt, geringere Exazerbationsrate mit Triple-Therapie bei höherer Zahl eosinophiler Granulozyten im Vergleich zur dualen Bronchodilatation.
00:20:05
Wie sieht es mit den Eosinophilen und der COPD aus? Die COPD ist eine chronischentzündliche Erkrankung. Hier spielen beide Zellarten, die neutrophilen und die eosinophilen Granulozyten, eine wichtige Rolle. Interessanterweise ist es nicht so, dass Eosinophile nur mit Asthma assoziert sind. Bei einem Drittel der COPD-Patientinnen und -Patienten sehen wir eine Sputum Eosinophilie in dem Sinne, dass diese Werte im Normalbereich erhöht sind. Wir wissen, dass es eine Korrelation zwischen den Eosinophilen im Sputum, dem Blut und dem Lungengewebe gibt. Warum ist das wichtig? Primäre Untersuchungen fanden darin statt, dass man über indiziertes Sputum festgestellt hat, dass die eosinophilen Granulozyten erhöht sind. Wir wissen aber, dass ein induziertes Sputum nichts ist, was im Praxisalltag praktikabel ist. Deshalb fand man heraus, dass es eine Korrelation zwischen der Eosinophilenzahl im Sputum und denen im Blut gibt. Aufgrund dieser Korrelation hilft uns die Bestimmung der Bluteosinophilen als Surrogatparameter, einen Rückschluss auf die Eosinophilen im Sputum schließen zu können. Wir haben gesehen, dass COPD-Patientinnen und -Patienten mit einer erhöhten Exazerbationsrate erhöhte Eosinophile haben. Sie haben ein erhöhtes Exazerbationsrisiko, sie haben einen stärkeren FEV1-Abfall. Sie haben dadurch ein besseres Ansprechen auf die Steroide, was wir gesehen haben, und sie haben eine geringere Pneumonierate. Das heißt, die Patientinnen und Patienten sind gefährdeter, aber besser zu behandeln. Daher ist es wichtig, dass wir die eosinophilen Granulozyten zur Therapieentscheidung heranziehen. Aufgrund der Methode, dass wir ein großes Blutbild benötigen, sind sie sehr einfach bestimmbar.
00:22:14
Schauen wir an der Stelle auf die Mortalitätsdaten aus den Guidelines. Es ist aufzuzeigen, dass die Mortalitätsdaten der IMPACT-Studie erstmalig 2020 in die GOLD-Empfehlung aufgenommen wurden und 2021 durch die Daten aus der ETHOS-Studie ergänzt wurden. Das heißt, die Evidenz aus der IMPACT-Studie konnte durch weitere Daten aus der ETHOS-Studie unterstützt und bestätigt werden. Es ist wichtig, dass eine Dreifachkombination die Mortalität jeglicher Ursache reduziert, verglichen mit einer lang wirksamen, dualen Bronchodilatation. Hier sehen Sie die Daten der ETHOS-Studie, die multizentrisch randomisiert sind, mit Doppelblind-Phase und Drei-Parallelgruppen-Studie. Es wurden über 8.000 Patientinnen und Patienten eingeschlossen. Sie sehen, dass anders als in der IMPACT-Studie, zwei verschiedene Arme genommen wurden mit unterschiedlichen Dosen beim inhalativen Steroid. Mit einer höheren Rate, mit 160 Mikrogramm im Vergleich zu 80, und mit einer niedrigeren im Vergleich zur dualen Bronchodilatation und Kombination aus einem inhalativen Steroid und einem lang wirksamen Betamimetikum. Ebenfalls über 52 Wochen, wie wir es davor gesehen hatten.
00:23:43
Die Einschlusskriterien sind gut vergleichbar und ähnlich. Sie sehen, COPD-Patientinnen und -Patienten 40 bis 80 Jahre, entsprechende FEV1, FC-Ratio, FEV1-Werte 25 bis 65 Prozent. Sie sehen mindestens zehn Packungsjahre, zwei inhalative Erhaltungstherapien zum Zeitpunkt des Screenings. Sie sehen vergleichbare oder identische Situationen hinsichtlich der Exazerbationen, wie wir es bei der IMPACT-Studie gesehen haben. Es gibt keine aktuelle Asthma-Diagnose oder eine Diagnose von Asthma fünf bis zehn Jahre davor. Erhöhte Bluteosinophile waren kein Einschlusskriterium. Auf die co-primären Endpunkte geschaut, jährliche Rate, moderate, schwere Exazerbationen, hier Triple-Therapie im Vergleich zur dualen Bronchodilatation beziehungsweise der Kombination aus inhalativen Steroiden und lang wirksamem Betamimetikum. Sekundäre Endpunkte, Lebensqualität bis zur ersten moderaten, schweren Exazerbation, gerade schwere Exazerbation. Als klassisch sekundärer Endpunkt ist die Zeit bis zum Tod jeglicher Ursache definiert.
00:25:08
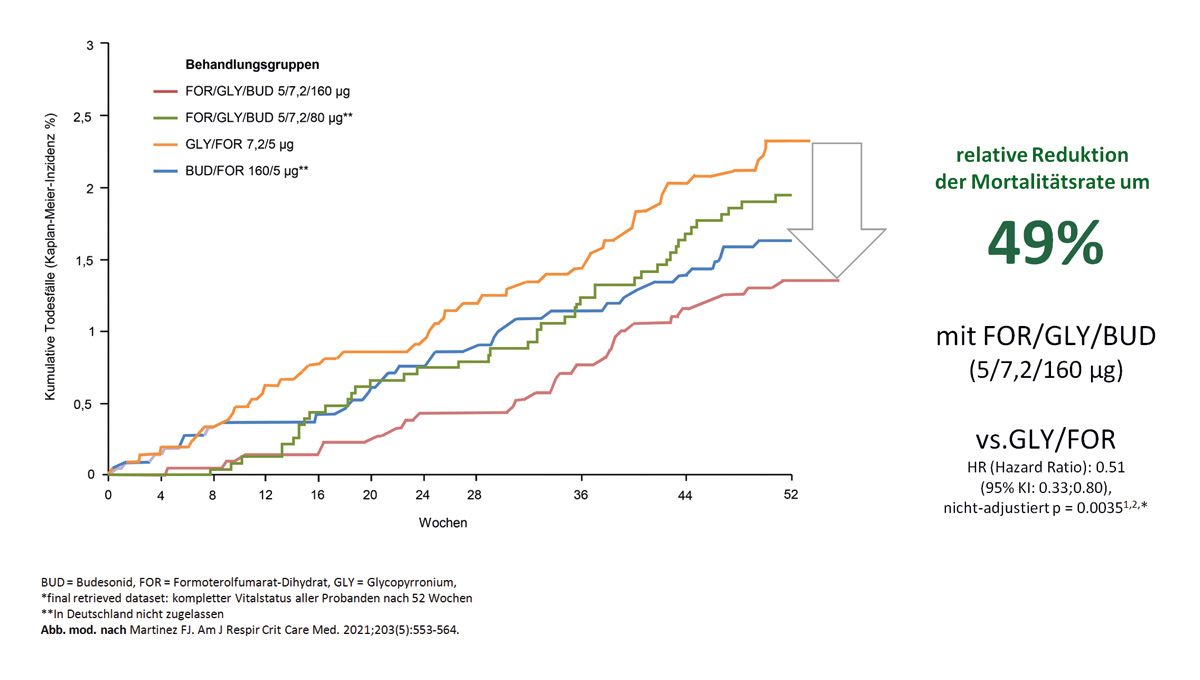
Schauen wir uns die Daten an, sehen wir vergleichbar, wie wir es in der IMPACT-Studie gesehen haben, eine relative Reduktion der Mortalitätsrate um 49 Prozent (Abb. 3).
Schauen wir uns die Triple-Therapie in der Hochdosis, ganz wichtig, im Vergleich mit der Kombinationstherapie aus dualer Bronchodilatation an. Hier ist hochdosiertes Steroid notwendig. Die niedrige Steroid-Dosis hat nicht dieses Ergebnis gebracht, jedenfalls nicht die Reduktion über 40. Der Vorteil war, dass man in der Studienpopulation versucht hat, im Nachgang weitere Zusatzuntersuchungen, ergänzende Sachen, durchzuführen. Man hat die Mortalitätsratensenkung nachberechnet und hat 49 Prozent gefunden. Das zweite ist, dass der Basiswert oder der Ausgangswert der Eosinophilen eine Rolle bei der Mortalität spielt. Das ist wichtig, da es da einen Zusammenhang gibt.
An dieser Stelle kommen wir zu dem spannenden Thema der jährlichen Exazerbationsrate und den Eosinophilenzahlen im Blut. Sie sehen beide Studien gegenüber dargestellt, die IMPACT-Studie auf der rechten Seite und die ETHOS-Studie. Sie sehen die verschiedenen Therapiearme dargestellt. Sie sehen, dass bei steigenden Eosinophilenzahlen die Anzahl der Exazerbationen deutlich, vor allem bei der dualen Bronchodilatation, gestiegen ist. Wenn bei diesen Patientinnen und Patienten eine Triple-Therapie durchgeführt wurde, unabhängig davon wie hoch diese Eosinophilen waren, hat dieser Einstieg bei beiden Studien deutlich geringer stattgefunden. Das heißt, dieser protektive Effekt der inhalativen Steroide in der Triple-Therapie ist sehr, sehr schön zu sehen. Sie sehen unten die blaue Linie, die das darstellt. Auf der anderen Seite sehen Sie den deutlichen Anstieg, wenn wir nur eine duale Bronchodilatation durchgeführt haben. Es sind vermehrt Exazerbationen aufgetreten, wenn kein inhalatives Steroid dabei war. Das Fazit ist, beide Studien zeigen, dass die Eosinophilenzahlen im Blut eine kontinuierliche Variable sind, die mit der Häufigkeit von Exazerbationen und dem Ansprechen von ICS zusammenhängen. Kommen wir zu einem weiteren wichtigen Thema, das ich schon angedeutet hatte, dem Zusammenhang zwischen den Eosinophilen und der Reduktion von kardiovaskulären Ereignissen in der ETHOS-Studie. Hier war es, dass bei den COPD-Patientinnen und -Patienten eine erhöhte Eosinophile hinsichtlich der Mortalität eine Rolle spielte.
00:28:18
Die Frage ist, hat die Therapie einen Einfluss auf kardiovaskuläre Ereignisse? Hier sehen Sie den Einfluss von Eosinophilen auf kardiovaskuläre Ereignisse. Das wirkt im ersten Moment unübersichtlich. Schauen wir genauer hin, haben wir auf der einen Seite die Gesamtheit bestätigter, schwerer kardialer Komplikationen. Sie sehen auf der rechten Seite den kardiovaskulären Tod. An der Stelle schauen wir uns auf der einen Seite die duale Bronchodilatation im Vergleich zur Triple-Therapie-Hochdosis an. Bei Patientinnen und Patienten, bei denen die Eosinophilen erhöht waren, war der protektive Effekt der inhalativen Steroide am größten. In diesem Diagramm an den Säulen auf der rechten Seite sehen Sie, dass in der Gruppe mit der dualen Bronchodilatation die kardiovaskulären Ereignisse am häufigsten waren. Das heißt, die Rate der schweren kardialen Komplikationen und der Tod durch das kardiovaskuläre Ereignis ist unter einer ICS-haltigen Therapie numerisch gesenkt worden. Wenn wir uns das anschauen, ist die Rate der Tode durch nichtfatale Myokardinfarkte unter der ICS-Therapie numerisch gesenkt worden. Sie sehen, wie deutlich schlechter die duale Bronchodilatation abschneidet und wir einen protektiven Effekt hinsichtlich der Triple-Therapie haben. Wie ist das Ganze zu sehen und zu beschreiben? In ETHOS und IMPACT ist dargestellt, dass die Triple-Therapie zur Mortalitätssenkung führt. Warum? Weil wir durch die Verhinderung der Exazerbationen die kardiovaskulären Ereignisse reduzieren können. Wir wissen, dass bei diesen Patientinnen und Patienten nach einer Exazerbation die Häufigkeit von kardiovaskulären Ereignissen und Schlaganfällen erhöht ist. Verhindern wir, dass es zu einer Exazerbation kommt, verhindern wir die Häufigkeit eines kardiovaskulären Ereignisses. Damit ist eine Reduktion der Mortalität zu erklären.
00:30:54
Schauen wir uns den Einsatz von ICS bei der COPD und die aktuellen Empfehlungen seitens GOLD an. Es ist zu sagen, dass bei COPD-Patientinnen und -Patienten mit einer Hospitalisierungsgeschichte aufgrund der COPD-Exazerbationen mit mehr als zwei moderaten COPD-Exazerbationen im Jahr oder einer Eosinophilenzahl gleich oder über 300 oder einer asthmatischen Mitkomponente eine ICS-Therapie empfohlen wird. Man sollte es in Erwägung ziehen bei Patientinnen und Patienten, die eine moderate Exazerbation pro Jahr hatten oder wenn die Eosinophilenzahl zwischen 100 bis 300 liegt. Man sollte eine ICS-Therapie nicht durchführen oder ablehnen, wenn wiederholt Pneumonien aufgetreten sind oder die Eosinophilen unter 100 sind. Sollten zusätzlich in der Anamnese mykobakterielle Infektionen eine Rolle spielen, sollte man auf das ICS in jedem Fall verzichten.
00:31:59
Wie sieht die Behandlung der exazerbierten Patientinnen und Patienten aus? Welche Maßnahmen können einen Einfluss auf das Mortalitätsrisiko nehmen? Wir wissen, was ich schon angedeutet hatte, dass wir bei der COPD eine Abwärtsspirale (Abb. 4) haben. Das heißt, die Lungenfunktion verschlechtert sich bei den Patientinnen und Patienten, die Exazerbationen steigen. Wir haben eine gehäufte Hospitalisierungsrate und das Ganze geht mit steigenden Exazerbationen, vermehrten Hospitalisierungen und mit einer hohen Mortalität einher.
Schauen wir auf unseren Patienten mit COPD und Exazerbationen zurück. Er hatte eine Belastungsdyspnoe, produktiven Husten, vor allem morgens. Er hatte zwei Exazerbationen in den letzten zwölf Monaten und über 300 eosinophile Granulozyten im Differenzialblutbild. Was war die Therapieeskalation, die durchgeführt wurde? Das ICS wurde als zusätzliche, antientzündliche Komponente hinzugenommen, um das Risiko für die Verschlechterung der Exazerbationen zu reduzieren. Durch diese Kombination der medikamentösen und nichtmedikamentösen Therapie, die bei solchen Patientinnen und Patienten erfolgen soll, versuchen wir, diese Abwärtsspirale bei der COPD zu bremsen. Die nichtmedikamentösen Maßnahmen sind sehr wichtig. Motivieren Sie Ihre Patientinnen und Patienten zu Lungensport und körperlicher Aktivität. Das ist wichtig, weil wir nur so eine Verbesserung erreichen können.
Wie können wir die Mortalität bei den COPD-Patientinnen und -Patienten beeinflussen? Wie können wir einen positiven Einfluss auf die Mortalität von COPD-Patientinnen und -Patienten nehmen (Tab. 1)? Was müssten wir tun? Was ist wichtig? Wichtig ist, bei unseren Patientinnen und Patienten die Adhärenz zu erreichen und die Komorbiditäten zu behandeln, danach zu schauen und gezielt vorzugehen. Die Rauchentwöhnung ist ein wichtiger Punkt, den wir nicht vergessen dürfen. Sind unsere Patientinnen und Patienten hypoxämisch und ist die Indikation gegeben, empfiehlt es sich, sie mit einer Sauerstofflangzeittherapie zu versorgen. Wir sollten die Begleitmaßnahmen, wie Atem- und Physiotherapie und Ernährungstherapie nutzen. Sollten unsere Patientinnen und Patienten respiratorische Insuffizienzen haben, ist es bei diesen Patientinnen und Patienten wichtig, Maßnahmen wie die nichtinvasive Beatmung ins Kalkül zu ziehen. Ich hatte mehrfach gesagt, dass körperliche Aktivität sehr, sehr wichtig für unsere Patientinnen und Patienten ist. Die Kondition und Leistungsfähigkeit können stabilisiert werden. Was wir nicht vergessen dürfen, sind die regelmäßigen Schutzimpfungen. Die Influenza-, Covid- und die Pneumokokken-Impfung sind die drei Impfungen, die unseren Patientinnen und Patienten zu empfehlen sind.
Tab. 1: Mortalität bei COPD positiv beeinflussen
-
- Adhärenz der Patientinnen und Patienten
- Behandlung der Komorbiditäten
- Rauchentwöhnung
- Sauerstoffbehandlung bei hypoxämischen Patientinnen und Patienten
- Nutzung von Begleitmaßnahmen wie Atem-, Physio- und ggf. Ernährungstherapie, z. B. nichtinvasive Ventilation
- Körperliche Aktivität
- Regelmäßige Schutzimpfungen – zum Beispiel gegen Grippe, COVID und Pneumokokken
Literatur
-
-
- Bafadhel M et al, European Respiratory Journal 2021 58: RCT208.
- Calverley PM et al. N Engl J Med. 2007;356(8):775-89.
- Global Initiative for Chronic Obstructive Lung Disease, Update 2023.
- Lipson DA et al. N Engl J Med. 2018; 378:1671-1680.
- Lipson DA et al. Am J Respir Crit Care Med. 2020;201,12:1508-1516.
- Mammen MJ et al ATS 2021 A224.
- Martinez FJ. Am J Respir Crit Care Med. 2021;203(5):553-564.
- Nationale VersorgungsLeitlinie COPD – 2. Auflage. Version 1. 2021.
- Pascoe S et al.Lancet Respir Med. 2019;7(9):745-756.
- Pascoe SJ et al. Eur Respir J 2016; 48: 320–330.
- Rabe KF et al. N Engl J Med. 2020;383(1):35-48 und Supplement.
- Rothnie K et al. Am J Respir Crit Care Med 2018; 198 (4):464–471.
- Suissa S et al. Thorax 2012; 67:957-63.
- Tashkin DP, Wechsler ME. Int J Chron Obstruct Pulmon Dis. 2018;13:335-349.
- Vestbo J et al. Lancet. 2016;387(10030):1817-26.
- Vogelmeier C et al. Pneumologie 2018; 72(04): 253-308.
- Wedzicha J et al. Am J Respir Crit Care Med. 2008;177(1):19-26.
-
Bildquellen
Titel: © Yakobchuk Olena – stock.adobe.com


Tutorielle Unterstützung
Die tutorielle Unterstützung der Fortbildungsteilnehmer erfolgt durch unseren ärztlichen Leiter Dr. med. Alexander Voigt in Zusammenarbeit mit der arztCME-Redaktion. Inhaltliche Fragen können über das Kommentarfeld, direkt per Mail an service@arztcme.de oder via Telefon unter Tel.: +49(0)180-3000759 gestellt werden. Inhaltliche Fragen werden von unserem ärztlichen Leiter bzw. nach Rücksprache mit diesem und evtl. dem Autor auch von der arztCME-Redaktion beantwortet.
Technischer Support
Der technische Support der arztCME-Online-Akademie erfolgt durch geschulte Mitarbeiterinnen und Mitarbeiter des Betreibers health&media GmbH unter der E-Mail-Adresse technik@arztcme.de oder via Telefon unter Tel.: 49(0)180-3000759.