Adhärenz in der Multiple Sklerose (MS)-Therapie – Update
Interessengebiete: Allgemeinmedizin und Innere Medizin, Neurologie
Die Langzeitbehandlung der Multiplen Sklerose (MS) kann nur dann wirksam sein, wenn Patienten gemeinsam getroffene Therapie-Vereinbarungen einhalten können und u. a. Arzttermine zu Kontrolluntersuchungen wahrnehmen. Eine suboptimale Adhärenz ist bei allen chronischen Krankheiten, wie auch bei MS, weit verbreitet. Bei MS nimmt die Adhärenz nach Therapiestart in den ersten Behandlungsjahren ab und ist mit einem erhöhten Schubrisiko sowie höheren Gesundheitskosten verbunden. Die Gründe für eine geringe Adhärenz sind vielfältig. Die World Health Organization (WHO) hat die Adhärenz-beeinflussenden Faktoren in fünf interagierende Dimensionen eingeteilt.
In dieser Fortbildung wird das Thema Adhärenz bei MS aus psychologischer und neurologischer Sichtweise beleuchtet. Dabei wird thematisiert, welche Faktoren speziell bei MS die Adhärenz gefährden und welche Maßnahmen wesentlich zur Förderung der Adhärenz beitragen können.
Wenn Sie das Video zur arztCME-Fortbildung herunterladen wollen, registrieren Sie sich bitte oder melden Sie sich an.
Kursinhalt
Inhaltsverzeichnis
Einleitung
Die Langzeitbehandlung der Multiplen Sklerose (MS) kann nur dann wirksam sein, wenn Patienten gemeinsam getroffene Therapie-Vereinbarungen einhalten können und u. a. Arzttermine zu Kontrolluntersuchungen wahrnehmen. Eine suboptimale Adhärenz ist bei allen chronischen Krankheiten, wie auch bei MS, weit verbreitet. Bei MS nimmt die Adhärenz nach Therapiestart in den ersten Behandlungsjahren ab und ist mit einem erhöhten Schubrisiko sowie höheren Gesundheitskosten verbunden. Die Gründe für eine geringe Adhärenz sind vielfältig. Die World Health Organization (WHO) hat die Adhärenz-beeinflussenden Faktoren in fünf interagierende Dimensionen eingeteilt.
In dieser Fortbildung wird das Thema Adhärenz bei MS aus psychologischer und neurologischer Sichtweise beleuchtet. Dabei wird thematisiert, welche Faktoren speziell bei MS die Adhärenz gefährden und welche Maßnahmen wesentlich zur Förderung der Adhärenz beitragen können.
Adhärenz: Definition
Die Begriffe Adhärenz und Compliance werden häufig synonym verwendet. „Adhärenz“ wird bevorzugt verwendet, da „Compliance“ eher beschreibt, dass der Patient passiv die Anweisungen des Arztes befolgt und der Behandlungsplan nicht auf einer therapeutischen Allianz oder einem Vertrag zwischen dem Patienten und dem behandelnden Arzt beruht. Der moderne mündige Patient soll eigene Wünsche miteinbringen und die Therapie mitgestalten [1, 2].
Adhärenz steht für eine gleichberechtigte Arzt-Patienten-Partnerschaft und enthält zusätzlich die Bereitschaft des Arztes, medizinische Anweisungen und Strategien auf die Wünsche und Bedürfnisse des Patienten abzustimmen. Arzt und Patient entwickeln gemeinsam Therapieziele und treffen Entscheidungen („Shared Decision Making“). Die gemeinsame Entscheidung und Gestaltung der Therapie setzt voraus, dass der Patient gut informiert ist über Krankheit, Ursachen und Therapieoptionen [1]. Der Begriff Persistenz wird im Zusammenhang mit Therapietreue verwendet. Er beschreibt die Beibehaltung einer Therapie über einen bestimmten Zeitraum [3].
Adhärenz – Definition (WHO 2003 [1])
„… der Grad der Übereinstimmung zwischen dem Verhalten einer Person einerseits (Einnahme von Medikation, Einhalten einer Diät und / oder Veränderungen im Lebensstil)
und
den im Konsens mit einem Gesundheitsdienstleister vereinbarten Empfehlungen andererseits.“
Bedeutung der Adhärenz bei MS
Die langfristige, regelmäßige und korrekte Einnahme von Arzneimitteln ist bei chronischen Krankheiten eine wesentliche Voraussetzung für den Therapieerfolg. Abgesehen von Wirksamkeitsverlusten mit vermehrter Schubaktivität und Progression der Erkrankung sowie damit einhergehenden häufigeren Arztbesuchen und vermehrten Krankenhausaufenthalten ist eine eingeschränkte Adhärenz auch mit einem Produktivitätsverlust assoziiert. In Deutschland werden die direkten und indirekten Kosten durch mangelnde Adhärenz auf 7,5-10 Milliarden Euro jährlich geschätzt (Stand 2011) [4].
Eine suboptimale Adhärenz bei der Behandlung wird generell bei chronischen Krankheiten wie beispielsweise Epilepsie, Hypertonie, Depression, Diabetes oder Asthma häufig beobachtet und ist nicht nur ein Phänomen bei MS. Laut WHO (2003) sind in Industrieländern im Durchschnitt nur etwa die Hälfte der Patienten mit chronischen Krankheiten therapieadhärent [1]. Bei MS wurden laut Literaturangaben Adhärenz- raten von 60-90 % festgestellt [5-7]. Im langjährigen Therapieverlauf nehmen sowohl Adhärenz als auch Persistenz bei Patienten mit MS deutlich ab. In einer retrospektiven Studie, die auf Daten einer US-amerikanischen Krankenversicherung basiert, nahm die Adhärenz über einen Zeitraum von drei Jahren nach Therapiebeginn von anfangs 82 % bis auf 66,5 % ab (Abb. 1), während die Therapieabbrüche im gleichen Zeitraum von 3,5 % auf 42 % zunahmen [6].
Der Einfluss der Adhärenz auf die Krankheitsaktivität bei MS-Patienten mit Interferon-Therapie wurde in einer retrospektiven Studie untersucht [7] (Abb. 2). Die Adhärenz wurde dabei als Anteil der Versorgungstage bestimmt (MPR: Medication Possession Ratio) und die Patienten je nach Adhärenz in Subgruppen klassifiziert. Adhärente Patienten (MPR ≥ 85 %) wiesen über drei Jahre ein geringeres Schubrisiko auf als nichtadhärente Patienten. Lag die Adhärenz unter 70 %, nahm das Schubrisiko der MS-Patienten signifikant zu im Vergleich zu den Patienten mit einer Adhärenzrate von 85 % oder mehr
[7] (Abb. 2).

Abb. 1: Die Therapie-Adhärenz bei Patienten mit MS nahm über drei Jahre ab Therapiebeginn kontinuierlich ab (modifiziert nach Yermakov et al. 2015 [6]); PDC (Proportion Days Covered): Anteil der mit Medikation abgedeckten Tage

Abb. 2: Korrelation von Adhärenz und Schubrisiko (modifiziert nach Steinberg et al. 2010 [7]); MPR (Medication Possession Ratio): Anteil der Versorgungstage
Neben der Zunahme der Krankheitsaktivität ist eine geringe Adhärenz auch mit einer erhöhten Inanspruchnahme von Ressourcen des Gesundheitssystems verbunden [6]. In einer Studie aus dem Jahr 2017 stellten die Autoren fest, dass nichtadhärente Patienten mit MS (Adhärenzrate ≤ 80 %) rund 6000 US$ jährliche Mehrkosten pro Patient verursachten im Vergleich zu adhärenten Patienten (Adhärenzrate > 80 %) [6]. Patienten mit höherer Adhärenz nahmen die Ressourcen des Gesundheitssystems weniger in Anspruch, hatten weniger Tage mit Arbeitsausfällen und niedrigere direkte als auch indirekte Kosten. Ein Anstieg der Adhärenz um 10 Prozentpunkte verringerte die Wahrscheinlichkeit eines stationären Aufenthalts oder einer Notaufnahme signifikant um 9-19 %, die Arbeitsausfalltage um 3-8 % und die direkten und indirekten Kosten um 3-5 %, je nach Nachbeobachtungszeitraum (alles p < 0,01).
Adhärenz: Fünf interagierende Dimensionen
Die Adhärenz ist ein multidimensionales Phänomen, das durch das Zusammenspiel vielfältiger Faktoren bestimmt wird. Die World Health Organization (WHO) hat den Adhärenz-beeinflussenden Faktoren fünf Dimensionen zugeordnet, von denen die patientenbezogenen Faktoren nur eine Determinante darstellen (Abb. 3) [1].
Krankheitsbezogene Faktoren
MS wird als die Krankheit der 1000 Gesichter bezeichnet und ist mit vielfältigen Symptomen verbunden [8]. Einige physische Beeinträchtigungen können die Adhärenz behindern. Beispielsweise erschweren Sehstörungen, wie verschwommenes Sehen und Doppelbilder, den Umgang mit Blistern bei der Tabletteneinnahme oder mit Spritzen bzw. Pens bei der Selbstinjektion. Auch Störungen der Feinmotorik, Koordination sowie Sensibilitätsstörungen stellen Adhärenz-Hürden dar.
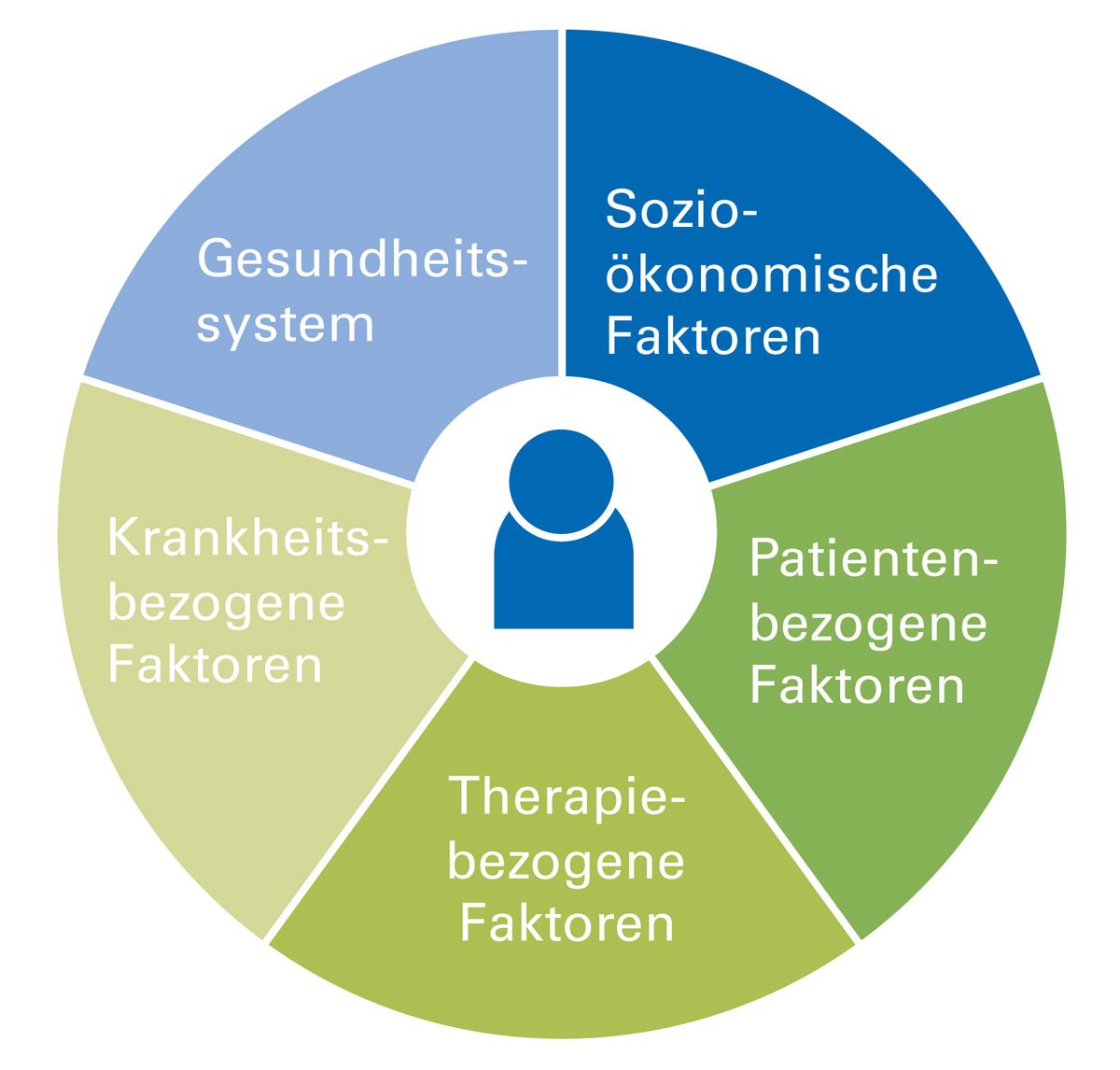
Abb. 3: Die fünf Dimensionen der Adhärenz-beeinflussenden Faktoren laut WHO (modifiziert nach WHO 2003 [1])
Aber nicht nur die sichtbaren Symptome der MS, sondern auch verborgene Symptome oder weiche Anzeichen beeinträchtigen die Adhärenz. Dazu gehören kognitive Funktionsstörungen, Fatigue, Depressionen und Angstzustände [9]. Diese Symptome stehen in der klinischen neurologischen täglichen Praxis nicht unbedingt im Fokus, aber wirken sich beim Patienten viel stärker auf die Lebensqualität und das tägliche Funktionieren aus als die körperlichen Symptome. Gedächtnisprobleme zählen zu den kognitiven Störungen bei MS, die sehr häufig zum Vergessen und damit zum Auslassen von Dosierungen führen [9]. Etwa 50 % der Patienten mit MS sind von Depressionen und Ängstlichkeit betroffen. Diese verborgenen Symptome haben nicht nur einen erheblichen Einfluss auf die Lebensqualität, sondern senken auch signifikant die Adhärenz bei MS [10].
Patientenbezogene Faktoren
Bewusste und unbewusste Erwartungen und Vorstellungen können die Wahrnehmung der Patienten beeinflussen. Die Erwartungen des Patienten stehen im Zusammenhang mit unzureichenden oder falschen Informationen über Arzneimittel und Ängsten vor Nebenwirkungen [1]. Geringe oder zu hohe Wirksamkeitserwartungen, Hoffnungslosigkeit und Frustration sind weitere Faktoren, die mit einer niedrigen Adhärenz verbunden sein können [1]. Bei Patienten mit MS sind mangelnde Kenntnisse zum Krankheitsbild ein wichtiger Risikofaktor dafür, die verlaufsmodifizierende Therapie zu unterbrechen oder ganz abzubrechen [11, 12].
Dagegen können umfassende Aufklärung, Wissen und Verständnis über die Krankheit das Vertrauen in die Therapie stärken und die gemeinsame Therapieentscheidung unterstützen. Dies kann die Motivation des Patienten erhöhen, adhärent zu bleiben und das Therapieziel nicht aus den Augen zu verlieren. Selbstmanagementfähigkeiten und Bewältigungsstrategien sind verhaltensbezogene Behandlungsziele, die zur Verbesserung der Adhärenz beitragen können [1]. Studienergebnisse belegen, dass die stärkere Beteiligung von Patienten bei medizinischen Entscheidungsprozessen mit einer höheren Behandlungszufriedenheit, einer verbesserten Adhärenz, mehr Wissen über die Krankheit, geringeren Entscheidungskonflikten, verbessertem Gesundheitsverhalten und einem verbesserten Gesundheitszustand verbunden ist [13].
Schlüssel zur Adhärenz: die Arzt-Patienten-Beziehung
Die vertrauensvolle Arzt-Patienten-Beziehung ist eine wichtige Säule für die Zufriedenheit der Patienten und für eine hohe Adhärenz. Die Offenheit für Patientenbedürfnisse und die patientenzentrierte Kommunikation ist die Basis, um Vertrauen aufzubauen [14]. Die Kommunikation mit Hilfe einer positiven Wortwahl kann eine positive Gesprächsatmosphäre schaffen. Botschaften werden eher angenommen, wenn sie in einen Gewinnrahmen eingebettet sind, also die positiven Folgen einer gewünschten Verhaltensänderung hervorheben (Gain Frames) [15, 16]. Menschen neigen dazu, Auswahlmöglichkeiten eher anzunehmen, wenn diese in einem positiven Rahmen präsentiert werden. Dagegen haben Furchtappelle vorwiegend kurzfristige Effekte und können auch zu Widerstand führen [16]. Eine gut realisierte partizipative Entscheidungsfindung kann bei Patienten zu mehr Wissen, realistischeren Erwartungen über den Krankheitsverlauf und zu einer höheren Zufriedenheit führen [17, 18].
Bausteine für die Arzt-Patienten-Kommunikation
- Gespräch auf Augenhöhe als Behandlungspartner („shared decision making“)
- Gemeinsame Absprachen treffen und Entscheidungen finden
- Vertrauen aufbauen
- Kommunikationsstil anpassen an die individuellen Patientenbedürfnisse
- Realistische Erwartungen schaffen
- Gain Frames nutzen (welche Vorteile bietet diese Therapie für diesen Patienten?)
- Positive Wortwahl
- Furchtappelle vermeiden
Die Neuroedukation vermittelt Krankheitsverständnis und Bewältigungsstrategien
Die Neuroedukation ist ein Konzept, um Patienten-Empowerment und Shared-Decision-Konzepte in den Versorgungsalltag zu integrieren [19]. Die Neuroedukation hilft Patienten mit chronischen ZNS-Erkrankungen, medizinische Fakten, Symptome und geeignete Coping-Strategien besser zu verstehen. Das bessere Verständnis führt zur besseren Akzeptanz der Krankheit und den Krankheitsfolgen. Die Stärkung der persönlichen Ressourcen erleichtert die Entwicklung von Bewältigungsstrategien und erhöht so die Teilhabefähigkeit. Neuroedukation hat weiterhin das Ziel, zur Selbsthilfe und einem gesundheitsförderlichen Verhalten anzuleiten sowie Strategien zur Verbesserung der Krankheitsaktivität zu vermitteln.
Bei der Neuroedukation werden Bestandteile aus Edukation, kognitiver Verhaltenstherapie (KVT) und erfahrungsbasierten Übungen kombiniert. Die wöchentlichen Kurse finden in Kleingruppen mit maximal zehn Teilnehmern statt, damit diese einen Nutzen aus dem Austausch mit anderen Betroffenen ziehen können [20].
Patientenbegleitprogramme unterstützen den Patienten auf vielfältige Weise
Im Rahmen von Patientenbegleitprogrammen (PSPs, Patient Support Programs) wird der individuelle Patient nach Registrierung durch einen (persönlichen) Coach (spezialisierte Fachkräfte, z. B. Krankenschwestern und -pfleger, Arzthelfer, Diätassistenten, Physiotherapeuten, Ergotherapeuten, Psychotherapeuten, Sportwissenschaftler etc.) von Beginn der Therapie an kontinuierlich begleitet und unterstützt. Dabei können die Aufklärung des Patienten vertieft, offene Fragen beantwortet und der Nutzen der Behandlung bekräftigt werden. Das Patientencoaching umfasst individuelle Telefongespräche (auch als „Videotelefonie“) zur Aufklärung der Multiplen Sklerose und der verordneten Therapie sowie zum Umgang mit möglichen Nebenwirkungen. Zielsetzung ist die Bewusstseinsförderung und Ermutigung des Patienten (Empowerment). PSPs nutzen dabei moderne Kommunikationsmedien, um eine individuelle Unterstützung im Umgang mit der Erkrankung anzubieten und damit die Lebensqualität und somit die Therapieadhärenz und die Persistenz nachhaltig zu verbessern [21, 22].
Zusätzlich stehen auch hilfreiche digitale Service-Angebote zur Verfügung, mit der Möglichkeit von Erinnerungsfunktionen zur Einhaltung der Dosierung der Medikation und von speziellen Vereinbarungen, Push-E-Mails, E-Learnings und Informationen zum Lifestyle mit Tipps zur Einhaltung einer gesunden Lebensweise usw. [22, 23] (Abb. 4). Ein signifikant positiver Effekt von PSPs auf die Adhärenz bei Patienten mit MS wurde in einer nichtinterventionellen Studie beobachtet. Die Adhärenz lag bei 93 % bei Patienten, die an einem PSP teilgenommen hatten, gegenüber 62 % bei Patienten, die kein PSP nutzten (p = 0,0197). Die unerwartet niedrige Inanspruchnahme von PSPs (8 %) limitiert jedoch die Aussagekraft dieses Ergebnisses [24]. Beobachtungen im Rahmen eines PSP zeigten, dass Patienten ohne Coaching mit 25,8 % häufiger eine DMF-Therapie nach zwölf Monaten abbrachen als Patienten mit Coaching (18,4 %). Die Abbruchquote wurde durch das Coaching um fast 30 % reduziert [24]. Intensiv versus weniger intensiv gecoachte MS-Patienten unter einer Therapie mit PegIFNβ-1a zeigten eine Abnahme von Therapie-Abbrüchen aufgrund von Nebenwirkungen von 45 % [25, 26].

Abb. 4: Patientenbegleitprogramme (PSPs) bieten Angebote zur Unterstützung der Patienten. (Abbildung adaptiert von https://mein.ms-life.de/service/gemeinsam-stark [22])
Sozioökonomische Faktoren
Sozioökonomische Faktoren beziehen sich auf die ökonomische und soziale Situation des Patienten, wie Bildungsgrad, Einkommen sowie das familiäre und private Umfeld bzw. die positiv erlebte Unterstützung [1, 2]. Eine gute Zusammenarbeit, Ausgeglichenheit und Rückhalt in der Familie gelten als adhärenzfördernd. Emotionale Überlastung und mangelnde Unterstützung können dagegen die Therapie-Adhärenz vermindern. Auch ein niedriger Bildungsgrad, geringes Einkommen und soziale Ausgrenzung kann sich negativ auf die Adhärenz auswirken [1]. Die sozioökonomische Situation des Patienten kann zwar nicht direkt verbessert werden, aber unterstützende Maßnahmen und Hilfestellungen sind für Patienten in ungünstigen Lebenssituationen besonders wichtig, z. B. in Form von PSPs und / oder Neuroedukation [20, 22, 24]. Zusätzlich können auch Angehörige als Adhärenz-Partner bei der Einhaltung der abgesprochenen Vereinbarungen miteinbezogen werden [23].
Therapiebezogene Faktoren
Die Therapielandschaft der MS hat sich in den letzten Jahren kontinuierlich erweitert [27]. Derzeit stehen in Deutschland 19 zugelassene krankheitsverändernde Medikamente (DMTs, disease-modifying therapies) zur Behandlung der MS zur Verfügung [28-30]. Die Erweiterung der Palette von oral und parenteral applizierbaren DMTs bietet Neurologen und MS-Patienten zum einen vielfältige Therapieoptionen, zum anderen sind die Entscheidungsprozesse komplexer [29, 30]. Neben Wirkmechanismen, Wirksamkeit, Applikationswegen und Dosierungen sind Nebenwirkungen, Langzeitsicherheit und das entsprechende Therapiemonitoring bei der Entscheidungsfindung zu berücksichtigen. Weitere Kriterien für die Therapie-Entscheidung sind: die individuelle Krankheitsaktivität, Prognosefaktoren für den jeweiligen Krankheitsverlauf, Alter, Situation des Patienten, Kinderwunsch und Patientenpräferenz [29, 30]. Inhalte des Patienten-Aufklärungsgesprächs sind neben den Therapiezielen und dem zu erwartenden Nutzen bzw. den möglichen Risiken durch einen Therapieverzicht auch mögliche Risiken, die durch Nebenwirkungen oder Rebound-Phänomene nach dem Absetzen einer Immuntherapie auftreten können [29].
Therapie-Monitoring als Adhärenz-Hürde
Aufgrund der vielfältigen Nebenwirkungsprofile der unterschiedlichen DMTs ist in der Regel ein engmaschiges Monitoring von unterschiedlichem Ausmaß je nach DMT vor, während und nach der MS-Therapie erforderlich (Abb. 5). Die DMTs wirken immunmodulierend oder immunsuppressiv. Nebenwirkungen können u. a. umfassen: Infektionen, Bradykardie, Herzblockaden, Infusionsreaktionen, Reaktionen an der Injektionsstelle, dermatologische Veränderungen, Veränderungen des Blutbildes sowie ophthalmologische (Makulaödeme), hepatische und gastroenterologische Komplikationen [28, 31]. Für bestimmte MS-Therapeutika wurde zudem eine mögliche Häufung neoplastischer Erkrankungen berichtet [32]. Mögliche infektiöse Risiken können Herpes-Virusinfektion, progressive multifokale Leukenzephalopathie (PML) oder andere opportunistische Infektionen umfassen. Vor dem Hintergrund einer umfassenden Adhärenz auf die jeweilige Behandlung, ist es wichtig, dass die Patienten vor der Therapie-Entscheidung über die Notwendigkeit und den Umfang des jeweiligen Monitorings aufgeklärt werden [29]. In den Entscheidungsprozess sollen die Patienten ihre persönlichen Präferenzen miteinbringen, die sich von den Präferenzen der behandelnden Ärzte deutlich unterscheiden können, wie eine Online-Umfrage im Rahmen eines Discrete-Choice-Experimentes mit MS-Patienten und niedergelassenen Ärzten ergab [33]. Idealerweise wird die Therapie-Entscheidung auf der Basis eines Patienten-Arzt-Konsens getroffen [29, 30].

Abb.5: Die Notwendigkeit und der Umfang des Monitorings vor, während und nach der Therapie kann eine Adhärenz-Hürde darstellen.
Weiterentwicklungen der MS-Therapie nach individuellen Patientenwünschen
Patientenwünschen. Die Einführung von oralen Substanzen, wie z. B. Teriflunomid und Dimethylfumarat, war ein erster wichtiger Meilenstein, nachdem zunächst über Jahrzehnte nur injizierbare MS-Therapieformen zur Verfügung standen und Patienten darunter zunehmend eine „Spritzenmüdigkeit“ oder Spitzenphobie entwickelten [29, 34, 35]. Eine andere Weiterentwicklung betraf die Pegylierung des Interferons IFNβ-1a. Die Pegylierung ist ein bewährtes Verfahren zur pharmakologischen Optimierung therapeutisch genutzter Proteine [36]. PegIFNß-1a wird verzögert renal ausgeschieden, weist dadurch eine längere Plasmahalbwertzeit und höhere IFN-Exposition auf. PegIFNβ-1a wird nur alle zwei Wochen verabreicht und ist für den Patienten damit anwendungsfreundlicher [37, 38]. Aufgrund der geringeren Applikationshäufigkeit kann die Verträglichkeit verbessert werden, d. h., die kumulierten Grippe-ähnlichen Symptome über vier Wochen wurden signifikant reduziert [39]. Aufgrund der Pegylierung konnte auch die Wirksamkeit verbessert werden [37, 38, 40]. Auch alternative Applikationswege können den Komfort erhöhen und die Berücksichtigung von individuellen Patientenwünschen ermöglichen. So ist Natalizumab beispielsweise inzwischen als Infusions- und subkutane Injektionstherapie erhältlich [41, 42] und PegIFNβ-1a kann subkutan und intramuskulär injiziert werden [28, 43].
Die jüngste Weiterentwicklung ist das neue Molekül Diroximelfumarat (DRF), das vergleichbar zu Dimethylfumarat (DMF) im Körper schnell zum aktiven Metaboliten Monomethylfumarat metabolisiert wird. DRF weist eine bessere gastrointestinale (GI) Verträglichkeit auf, da bei der DRF-Metabolisierung das Nebenprodukt Methanol zu 90 % weniger gebildet wird. Patienten berichten über eine höhere Lebensqualität aufgrund weniger Beeinträchtigungen in ihrem täglichen Leben und der Arbeitsfähigkeit aufgrund von GI-Ereignissen [44-46].
Zukünftig sind neue pharmakologische Optimierungen und Erweiterungen des therapeutischen Spektrums bei MS zu erwarten. Es ist daher zu hoffen, dass sich die zunehmend individualisierter werdende Therapie positiv auf Patientenzufriedenheit und Adhärenz auswirken wird.
Das Gesundheitssystem
Das System des Gesundheitswesens hat einen wesentlichen Einfluss auf die Adhärenz. Auch wenn die Gesundheitsversorgung in Deutschland im internationalen Vergleich relativ gut aufgestellt ist, gibt es einige Aspekte des Gesundheitssystems, die sich negativ auf die Adhärenz auswirken, wie überlastete Fachärzte, lange Wartezeiten, kurze Sprechzeiten und fehlende Anreize zur Durchführung von Adhärenz-steigernden Maßnahmen. Adhärenz-fördernde Maßnahmen des Gesundheitssystems sind dagegen: eine vertrauensvolle Arzt-Patienten-Beziehung, Abbau von Arbeitsüberlastung, ärztli- che Fortbildungen und finanzielle Anreize zum Thema Adhärenz und die Förderung von Maßnahmen (z. B. PSPs oder Neuroedukation) zur individuellen Unterstützung der Patienten [1, 49].
Fazit
Eine hohe Adhärenz ist eine wichtige Voraussetzung für den Erfolg der MS-Therapie. Eine suboptimale Adhärenz ist bei MS, wie auch bei anderen chronischen Krankheiten, weit verbreitet und geht mit einem erhöhten Schubrisiko, einer Progression der Erkrankung und höheren Kosten einher. Die Adhärenz basiert auf dem Zusammenspiel unter- schiedlicher Faktoren, die laut WHO in fünf Dimensionen klassifiziert werden: krankheitsbezogene, patientenbezogene, therapiebezogene, sozioökonomische und Gesundheitssystem-Faktoren.
Krankheitsbezogene Faktoren bei MS umfassen physische Komponenten, wie z. B. Seh- und Koordinationsstörungen, und psychische Symptome, wie kognitive Störungen, Fatigue, Depression und Ängstlichkeit. Diese können leicht übersehen werden und haben sogar einen größeren Einfluss auf Lebensqualität und Adhärenz.
Patientenbezogene Faktoren basieren auf bewussten und unbewussten Wahrnehmungen des Patienten. Auswirkungen auf die Adhärenz zeigen die jeweilige Haltung des Patienten, das individuelle Wissen um die Erkrankung und die Behandlung sowie die Arzt-Patienten-Beziehung. Die patientenzentrierte Kommunikation ist ein Schlüssel, um Vertrauen aufzubauen. Der Patient wird in Therapieentscheidungen unter Berücksichtigung der individuellen Patientenpräferenzen miteingebunden. Patientenbegleitprogramme (PSPs) und Neuroedukation sind adhärenzfördernde Konzepte zur Vermittlung von Krankheitsverständnis und Coping-Strategien im Versorgungsalltag, die insbeson- dere zur Unterstützung von Patienten mit ungünstigen sozioökonomischen Faktoren hilfreich sind. PSPs beinhalten auch digitale Service-Angebote und nützliche Apps, z. B. zur Erinnerung an Arzttermine.
Ein komplexes Therapie-Regime, häufige Applikationen, viele Nebenwirkungen und ein aufwendiges Monitoring sind therapiebezogene Faktoren, die sich auf die Adhärenz auswirken können. Weiterentwicklungen der MS-Therapeutika in den letzten Jahren haben maßgeblich zur Verbesserung von Komfort und Auswahlmöglichkeiten beigetragen. Orale DMTs, alternative Applikationsmöglichkeiten sowie neue Prodrug-Moleküle, wie z. B. Diroximelfumarat mit verbesserter GI-Verträglichkeit, können zunehmend eine Therapie nach individuellen Patientenwünschen ermöglichen.
Die Adhärenz bei MS ergibt sich insgesamt aus dem komplexen Zusammenspiel von vielen sich beeinflussenden Faktoren, die sich durch psychologische und neurologische Stellschrauben verbessern lassen. Neben weiterentwickelten MS-Therapeutika sind Aufklärung, Einbeziehung, Ermutigung und Unterstützung der Patienten die wichtigsten Eckpfeiler für die Stärkung der Adhärenz bei MS.
Abkürzungen
ARR Annualized relapse rate (Jährliche Schubrate)
CME Continuing Medical Education
DGN Deutsche Gesellschaft für Neurologie
DMF Dimethylfumarat
DMTs Disease-modifying therapies (Krankheitsmodifizierende Therapien)
EDSS Expanded Disability Status Scale
i.m. intramuskulär
IFN Interferon
IFNβ Interferon beta
kDa Kilodalton
KI Konfidenzintervall
MS Multiple Sklerose
MPR Medication Possession Ratio (Quotient aus Versorgungstagen durch Therapietage)
PEG Polyethylenglykol
PDC Proportion Days Covered (Anteil der durch DMT abgedeckten Tage)
PSPs Patient Support Programs (Patientenbegleitprogramme)
s.c. subkutan
TNF-α Tumornekrosefaktor-alpha
vs. versus
WHO World Health Organization
ZNS Zentrales Nervensystem
Literatur
- World Health Organization (WHO). Adherence to long-term therapies. (2003). http://apps.who.int/iris/bitstream/handle/10665/42682/9241545992.pdf;jsessionid=C87A012E244996A29753C9F9B0FEBF5A?sequence=1
- Osterberg L, Blaschke T (2005) Adherence to medication. N Engl J Med 353 (5):487-497. doi:10.1056/NEJMra050100
- Cramer JA, Roy A, Burrell A et al. (2008) Medication compliance and persistence: terminology and definitions. Value Health 11 (1):44-47. doi:10.1111/j.1524 4733.2007.00213.x
- Laufs U, Böhm M, Kroemer HK et al. (2011) [Strategies to improve medication adherence]. Dtsch Med Wochenschr 136 (31-32):1616-1621. doi:10.1055/s-0031-1281566
- Costello K, Kennedy P, Scanzillo J (2008) Recognizing nonadherence in patients with multiple sclerosis and maintaining treatment adherence in the long term. Medscape J Med 10 (9):225
- Yermakov S, Davis M, Calnan M et al. (2015) Impact of increasing adherence to disease-modifying therapies on healthcare resource utilization and direct medical and indirect work loss costs for patients with multiple sclerosis. J Med Econ 18 (9):711-720. doi:10.3111/13696998.2015.1044276
- Steinberg SC, Faris RJ, Chang CF, Chan A, Tankersley MA (2010) Impact of adherence to interferons in the treatment of multiple sclerosis: a non-experimental, retrospective, cohort study. Clin Drug Investig 30 (2):89-100. doi:10.2165/11533330-000000000-00000
- Giovannoni G, Butzkueven H, Dhib-Jalbut S et al. (2016) Brain health: time matters in multiple sclerosis. Mult Scler Relat Disord 9 Suppl 1:S5-s48. doi:10.1016/j.msard.2016.07.003
- Penner IK (2016) Evaluation of cognition and fatigue in multiple sclerosis: daily practice and future directions. Acta Neurol Scand 134 Suppl 200:19-23. doi:10.1111/ane.12651
- Washington F, Langdon D (2021) Factors affecting adherence to disease-modifying therapies in multiple sclerosis: systematic review. J Neurol. doi:10.1007/s00415-021-10850-w
- Remington G, Rodriguez Y, Logan D, Williamson C, Treadaway K (2013) Facilitating medication adherence in patients with multiple sclerosis. Int J MS Care 15 (1):36-45. doi:10.7224/1537-2073.2011-038
- Kip M, Schönfelder T, H.H. B (2016) Weißbuch Multiple Sklerose. Springer-Verlag Berlin Heidelberg
- Stacey D, Légaré F, Lewis K et al. (2017) Decision aids for people facing health treatment or screening decisions. Cochrane Database Syst Rev 4 (4):Cd001431. doi:10.1002/14651858.CD001431.pub5
- Härter M, Dirmaier J (2020) 4.3. Arzt-Patient-Kommunikation. In: Deinzer R, von dem Knesebeck O (eds) Online Lehrbuch der Medizinischen Psychologie und Medizinischen Soziologie. German Medical Science GMS Publishing House, Berlin. doi:10.5680/OLMPS000062
- Barnes K, Faasse K, Geers AL et al. (2019) Can Positive Framing Reduce Nocebo Side Effects? Current Evidence and Recommendation for Future Research. Frontiers in Pharmacology 10. doi:10.3389/fphar.2019.00167
- Seehausen M, Hänel P (2011) Arzt-Patienten-Kommunikation: Adhärenz im Praxisalltag effektiv fördern. Dtsch Arztebl Int 108 (43):A-2276 / B-1918
- KBV: Arzt-Patienten-Kommunikation. (2021). https://www.kbv.de/media/sp/Arzt-Patienten-Kommunikation.pdf
- Härter M Patientenzentrierte Kommunikation und partizipative Entscheidungsfindung in der Onkologie. https://www.springermedizin.de/emedpedia/kompendium-internistische onkologie/patientenzent- rierte-kommunikation-und-partizipative-entscheidungsfindung-in-der-onkologie?epediaDoi=10.1007 %2F978-3-662-46764-0_354
- Meier U, Penner IK (2017) Neuroedukation muss in die Versorgung. NeuroTransmitter 28 (S1)
- Penner IK, Meier U (2018) Evaluation von Neuroedukation. Neurotransmitter 29 (S1)
- Ries S, Elias WG, Japp G, Lang M (2008) Improvement of adherence in MS therapy – results of an MS therapy support study. Nervenheilkunde 27 (09):818-922
- Dein MS-Begleitprogramm. https://mein.ms-life.de/service/gemeinsam-stark/.
- Zehn Vorschläge zur Verbesserung der Adhärenz in der Arzneimitteltherapie (2014). AMB 48 (40DB01)
- Lenz F, Harms L (2020) The Impact of Patient Support Programs on Adherence to Disease-Modifying Therapies of Patients with Relapsing-Remitting Multiple Sclerosis in Germany: A Non-Interventional, Prospective Study. Adv Ther 37 (6):2999-3009. doi:10.1007/s12325-020-01349-3
- Niemczyk G, Begus-Nahrmann Y, Washeim N et al. (2018) Real-world characterisation of peginterferon beta-1a asso- ciated flu-like symptoms and injection site reactions and impact of mitigation strategies coached in an individualized patient support program in Germany. Paper presented at the ECTRIMS-ACTRIMS,
- Begus-Nahrmann Y, Abel J, Niemczyk G et al. (2017) Hands on experience in therapy management and challenges addressed in an individualized patient support program of three different therapeutic disease-modifying approaches to treat Multiple Sclerosis in Germany.
- Piehl F (2021) Current and emerging disease-modulatory therapies and treatment targets for multiple sclerosis. J Intern Med 289 (6):771-791. doi:10.1111/joim.13215
- Fachinformation. www.fachinfo.de
- Wiendl H, Gold R, Berger T et al. (2021) [Multiple sclerosis treatment consensus group (MSTCG): position paper on disease-modifying treatment of multiple sclerosis 2021 (white paper)]. Nervenarzt 92 (8):773-801. doi:10.1007/ s00115-021-01157-2
- Hemmer B et al. Diagnose und Therapie der Multiplen Sklerose, Neuromyelitis-optica-Spektrum-Erkrankungen und MOG-IgG-assoziierten Erkrankungen, S2k-Leitlinie, 2021, in: Deutsche Gesellschaft für Neurologie (Hrsg.), Leitlinien für Diagnostik und Therapie in der Neurologie. . www.dgn.org/leitlinien.
- Kompetenznetzwerk Multiple Sklerose. Qualitätshandbuch MS / NMOSD. Empfehlungen zur Therapie der Multiplen Sklerose / Neuromyelitis-optica-Spektrum-Erkrankungen für Ärzte. 2021.
- McGinley MP, Goldschmidt CH, Rae-Grant AD (2021) Diagnosis and Treatment of Multiple Sclerosis: A Review. Jama 325 (8):765-779. doi:10.1001/jama.2020.26858
- Poulos C, Wakeford C, Kinter E et al. (2020) Patient and physician preferences for multiple sclerosis treatments in Germany: A discrete-choice experiment study. Mult Scler J Exp Transl Clin 6 (1):2055217320910778. doi:10.1177/2055217320910778
- Kleinschnitz C, Niemczyk G, Rehberg-Weber K, Wernsdörfer C (2015) Interferon Beta-1a as a Treatment Option for Untreated Patients with Multiple Sclerosis (AXIOM): A Prospective, Observational Study. Int J Mol Sci 16 (7):15271-15286. doi:10.3390/ijms160715271
- Devonshire V, Lapierre Y, Macdonell R et al. (2011) The Global Adherence Project (GAP): a multicenter observational study on adherence to disease-modifying therapies in patients with relapsing-remitting multiple sclerosis. Eur J Neurol 18 (1):69-77. doi:10.1111/j.1468-1331.2010.03110.x
- Pasut G, Veronese FM (2012) State of the art in PEGylation: the great versatility achieved after forty years of research. J Control Release 161 (2):461-472. doi:10.1016/j.jconrel.2011.10.037
- Calabresi PA, Kieseier BC, Arnold DL et al. (2014) Pegylated interferon β-1a for relapsing-remitting multiple sclerosis (ADVANCE): a randomised, phase 3, double-blind study. Lancet Neurol 13 (7):657-665. doi:10.1016/ s1474-4422(14)70068-7
- Coyle PK, Shang S, Xiao Z, Dong Q, Castrillo-Viguera C (2018) Matching-adjusted comparisons demonstrate better clinical outcomes with SC peginterferon beta-1a every two weeks than with SC interferon beta-1a three times per week. Mult Scler Relat Disord 22:134-138. doi:10.1016/j.msard.2018.02.021
- Naismith RT, Hendin B, Wray S et al. (2019) Patients transitioning from non-pegylated to pegylated interferon beta-1a have a low risk of new flu-like symptoms: ALLOW phase 3b trial results. Mult Scler J Exp Transl Clin 5 (1):2055217318822148. doi:10.1177/2055217318822148
- Newsome SD, Scott TF, Arnold DL et al. (2018) Long-term outcomes of peginterferon beta-1a in multiple sclerosis: results from the ADVANCE extension study, ATTAIN. Ther Adv Neurol Disord 11:1756286418791143. doi:10.1177/1756286418791143
- Plavina T, Fox EJ, Lucas N, Muralidharan KK, Mikol D (2016) A Randomized Trial Evaluating Various Administration Routes of Natalizumab in Multiple Sclerosis. J Clin Pharmacol 56 (10):1254-1262. doi:10.1002/jcph.707
- Trojano M, Ramió-Torrentà L, Grimaldi LM et al. (2021) A randomized study of natalizumab dosing regimens for relapsing-remitting multiple sclerosis. Mult Scler 27 (14):2240-2253. doi:10.1177/13524585211003020
- Zhao Y, Chen K, Ramia N et al. (2021) Bioequivalence of intramuscular and subcutaneous peginterferon beta-1a: results of a phase I, open-label crossover study in healthy volunteers. Ther Adv Neurol Disord 14:1756286420975227. doi:10.1177/1756286420975227
- Naismith RT, Wundes A, Ziemssen T et al. (2020) Diroximel Fumarate Demonstrates an Improved Gastrointestinal Tolerability Profile Compared with Dimethyl Fumarate in Patients with Relapsing-Remitting Multiple Sclerosis: Results from the Randomized, Double-Blind, Phase III EVOLVE-MS-2 Study. CNS Drugs 34 (2):185-196. doi:10.1007/ s40263-020-00700-0
- Palte MJ, Wehr A, Tawa M et al. (2019) Improving the Gastrointestinal Tolerability of Fumaric Acid Esters: Early Findings on Gastrointestinal Events with Diroximel Fumarate in Patients with Relapsing-Remitting Multiple Sclerosis from the Phase 3, Open-Label EVOLVE-MS-1 Study. Adv Ther 36 (11):3154-3165. doi:10.1007/s12325-019-01085-3
- Naismith R, Wolinsky J, Jasinska E et al. (2020) P272. Paper presented at the ACTRIMS, Florida
- Abuchowski A, van Es T, Palczuk NC, Davis FF (1977) Alteration of immunological properties of bovine serum albumin by covalent attachment of polyethylene glycol. J Biol Chem 252 (11):3578-3581
- Hu X, Miller L, Richman S et al. (2012) A novel PEGylated interferon beta-1a for multiple sclerosis: safety, pharmaco- logy, and biology. J Clin Pharmacol 52 (6):798-808. doi:10.1177/0091270011407068
- HTA-Bericht 65: Maßnahmen zur Verbesserung der Compliance bzw. Adherence in der Arzneimitteltherapie mit Hinblick auf den Therapieerfolg. https://portal.dimdi.de/de/hta/hta_berichte/hta206_bericht_de.pdf
Bildquellen
Titel:
© Monster_Design – stock.adobe.com
© Aha-Soft – stock.adobe.com
© Afanasiev Oleksii – stock.adobe.com
Abb. 5:
© Monster_Design – stock.adobe.com
© Aha-Soft – stock.adobe.com
© Afanasiev Oleksii – stock.adobe.com



Tutorielle Unterstützung
Die tutorielle Unterstützung der Fortbildungsteilnehmer erfolgt durch unseren ärztlichen Leiter Dr. med. Alexander Voigt in Zusammenarbeit mit der arztCME-Redaktion. Inhaltliche Fragen können über das Kommentarfeld, direkt per Mail an service@arztcme.de oder via Telefon unter Tel.: +49(0)180-3000759 gestellt werden. Inhaltliche Fragen werden von unserem ärztlichen Leiter bzw. nach Rücksprache mit diesem und evtl. dem Autor auch von der arztCME-Redaktion beantwortet.
Technischer Support
Der technische Support der arztCME-Online-Akademie erfolgt durch geschulte Mitarbeiterinnen und Mitarbeiter des Betreibers health&media GmbH unter der E-Mail-Adresse technik@arztcme.de oder via Telefon unter Tel.: 49(0)180-3000759.