Auf dem DKK 2026 wurde auch die Zukunft der onkologischen Prävention diskutiert. Die zentrale Frage lautet nicht mehr, ob wir Krebs früher erkennen können, sondern wie wir vorhandenes Wissen konsequent und gerecht in Versorgungssysteme integrieren.
Krebs bleibt eine der größten gesundheitspolitischen Herausforderungen in Deutschland. Jährlich werden rund 520.000 Neuerkrankungen diagnostiziert, etwa 230.000 Menschen sterben an den Folgen einer malignen Erkrankung. Prognosen gehen aufgrund der demografischen Entwicklung von weiter steigenden Inzidenzen aus.
Gleichzeitig ist seit Jahren bekannt, dass ein erheblicher Anteil dieser Erkrankungen vermeidbar wäre. Schätzungen zufolge könnten etwa 37–40 % aller Krebsneuerkrankungen durch konsequente Primärprävention verhindert werden. In Kombination mit strukturierter Früherkennung (Sekundärprävention) ließen sich sogar bis zu 60 % der Krebstodesfälle vermeiden – auf Basis des bereits vorhandenen Wissens.
Die wesentlichen modifizierbaren Risikofaktoren sind ja seit Jahrzehnten bekannt: Tabakkonsum, ungesunde Ernährung, Adipositas, Bewegungsmangel, Alkoholkonsum, onkogene Infektionen. Trotz dieser klaren Evidenz bleibt die Implementierung auf Bevölkerungsebene unzureichend. Gleichzeitig fließt nur ein geringer Anteil der Gesundheitsausgaben in strukturierte Präventionsstrategien, während der Großteil in kurative Versorgung investiert wird.
Von „One size fits all“ zur risikoadaptierten Prävention
Traditionelle Screeningprogramme orientieren sich primär am Lebensalter. Beispielhaft ist die Darmkrebsvorsorge ab dem 50. Lebensjahr. Dieses altersbasierte Modell ignoriert jedoch die multidimensionale Natur des Krebsrisikos. Denn das individuelle Risiko wird auch bestimmt durch genetische Disposition, Geschlecht, Lebensstil und Komorbiditäten. Die Zukunft liegt in der Verschiebung von einer altersbasierten zu einer risikobasierten Präventionslogik.
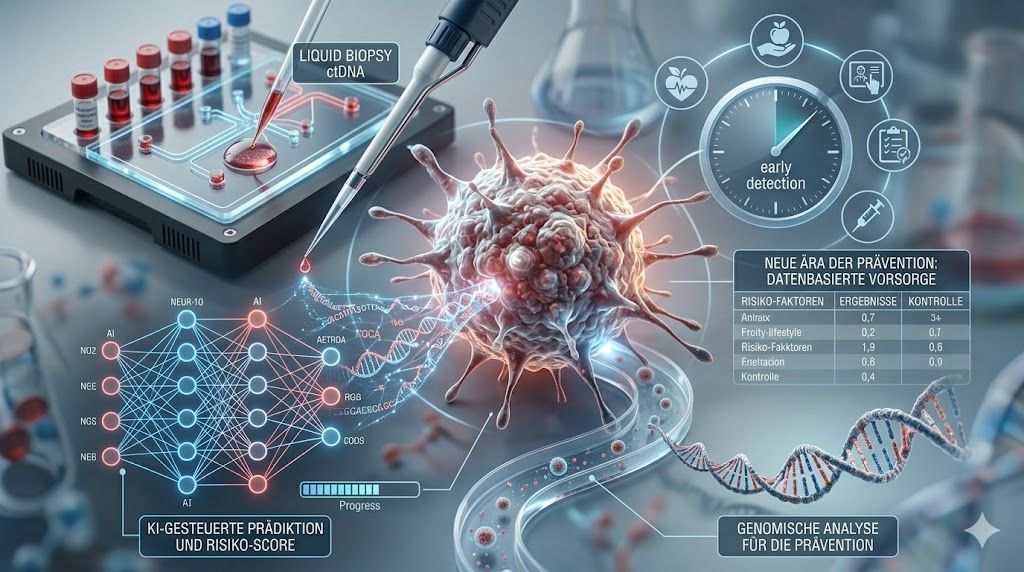
Ein wesentlicher Innovationsbereich ist die molekulare Früherkennung mittels Liquid Biopsy. Tumoren setzen zellfreie DNA-Fragmente (ctDNA) in den Blutkreislauf frei, die mit hochsensitiven Sequenziermethoden erfasst werden können. Vision ist die Detektion maligner Prozesse vor klinischer Manifestation.
Herausforderungen bestehen weiterhin hinsichtlich der Sensitivität in Frühstadien, der Spezifität bei altersassoziierten Mutationen (z. B. klonale Hämatopoese sowie der gesundheitsökonomischen Skalierbarkeit. Dennoch markiert die Liquid Biopsy einen potenziellen Wendepunkt in der Sekundär- und Tertiärprävention.
Auch KI-basierte Systeme finden zunehmend Eingang in die klinische Prävention: KI-gestützte Koloskopiesysteme erhöhen die Adenomdetektionsrate und verbessern die Differenzierung zwischen neoplastischen und nicht-neoplastischen Läsionen. In der Dermatologie ermöglichen
Algorithmen zur Bildanalyse eine standardisierte Risikostratifizierung von Hautläsionen. Und elektronische Gesundheitsdaten können genutzt werden, um individuelle Krankheitswahrscheinlichkeiten vorherzusagen und personalisierte Screeningstrategien abzuleiten.
Die Stärkung der biologischen Resilienz ist ein komplett neuer Ansatz. Hintergrund: Mit zunehmendem Alter nimmt die Immunkompetenz ab. Gleichzeitig steigt die Inzidenz maligner Erkrankungen. Innovative Forschungsansätze zielen darauf ab, das alternde Immunsystem gezielt zu stärken. Experimentelle Konzepte umfassen mRNA-basierte Strategien zur Expression thymusspezifischer sowie die Verbesserung der immunologischen Tumorüberwachung. Diese immunologischen Ansätze verschieben Prävention von passiver Vermeidung hin zu aktiver biologischer Resilienzsteigerung.
Implementierung: Die eigentliche Systemherausforderung
Doch technologische Innovation allein reicht nicht aus. Ein Beispiel ist die HPV-Impfung. Hier haben wir hohe Wirksamkeit und eine robuste Evidenz – dennoch unzureichende Impfquoten. Es zeigt sich die zentrale Implementierungslücke zwischen wissenschaftlicher Erkenntnis und populationsweiter Anwendung. Prävention ist daher nicht nur eine medizinische, sondern auch eine gesellschaftliche Aufgabe.
Die zukünftige Krebsprävention wird sich daher entlang mehrerer Entwicklungslinien entfalten. Die zentrale Frage lautet nicht mehr, ob wir Krebs früher erkennen können, sondern wie wir vorhandenes Wissen konsequent und gerecht in Versorgungssysteme integrieren. Die Zukunft der Prävention beginnt nicht im Labor. Sie beginnt in der Umsetzung.
Text: Reinhard Merz
Bild: Google Nano Banana für arztCME