Sprunggelenk: Verletzungen, akute Krankheitsbilder und ihre Therapie
Interessengebiete: Allgemeinmedizin und Innere Medizin, Chirurgie, Orthopädie, Rheumatologie
Verletzungen des Sprunggelenks treten im Rahmen sportlicher Aktivitäten besonders häufig auf. Oft sind Frakturen und Bandverletzungen die Folge. Aber auch chronische Erkrankungen wie Arthrose oder Knorpelschaden, Osteochondrosis dissecans sowie das Tibialis-posterior-Syndrom können die Funktion des Sprunggelenks beeinträchtigen. Bandverletzungen werden meist konservativ behandelt. Bei Frakturen ist die konservative Therapie bei nicht-dislozierten Verhältnissen möglich. In schwereren Fällen ist eine Operation notwendig, wie zum Beispiel eine Osteosynthese. Orthopädietechnische Hilfsmittel spielen sowohl nach einer Operation als auch im konservativen Behandlungssetting eine wichtige Rolle.
Kursinhalt
Inhaltsverzeichnis
Einleitung
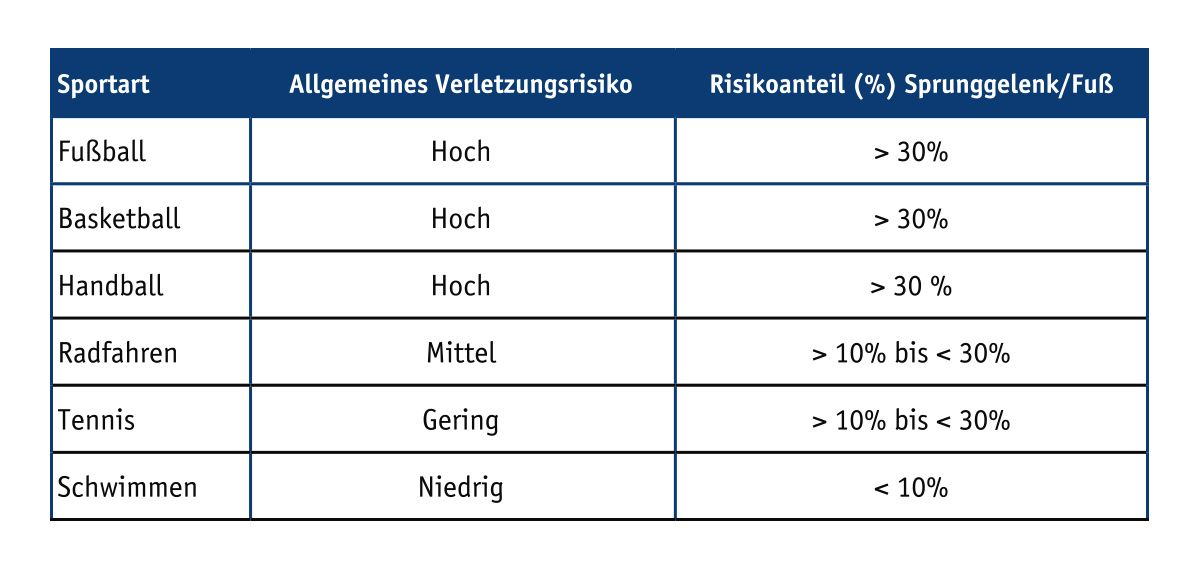
Das Sprunggelenk ist in etwa 30 bis 50 % aller Sportverletzungen involviert. Im Rahmen sportlicher Aktivitäten treten Verletzungen besonders häufig z. B. durch Umknicken des Fußes beim Laufen oder durch einen kräftigen Aufprall infolge eines hohen Sprungs auf. Die starke Abhängigkeit des Risikos für Sprunggelenksverletzungen von der jeweils ausgeübten Sportart ist in Tabelle 1 dargestellt. Da das Sprunggelenk seine enorme Stabilität erst durch das komplexe Zusammenspiel von ossären Gelenkbestandteilen und umliegenden Weichteilen erlangt, handelt es sich oftmals um Kombinationsverletzungen. Hierbei zählen Distorsionen, Frakturen und Verletzungen der stabilisierenden Bandapparate zu den häufigsten akuten Sprunggelenksverletzungen [1, 2]. Das zweite Modul dieser Fortbildungsreihe befasst sich mit den Krankheitsbildern des oberen und unteren Sprunggelenks, insbesondere den Frakturen und Bandverletzungen, und zeigt die aktuellen Therapiemöglichkeiten auf. Darüber hinaus werden Knorpelschaden im oberen Sprunggelenk (OSG), Osteochondrosis dissecans (OD) sowie das Tibialis-posterior-Syndrom thematisiert.
Tab. 1: Prozentualer Risikoanteil von Sprunggelenks- und Fußverletzungen an der Gesamtheit aller Sportverletzungen [modifiziert nach 3]
Frakturen des Sprunggelenks
Klassifikation von Sprunggelenksfrakturen
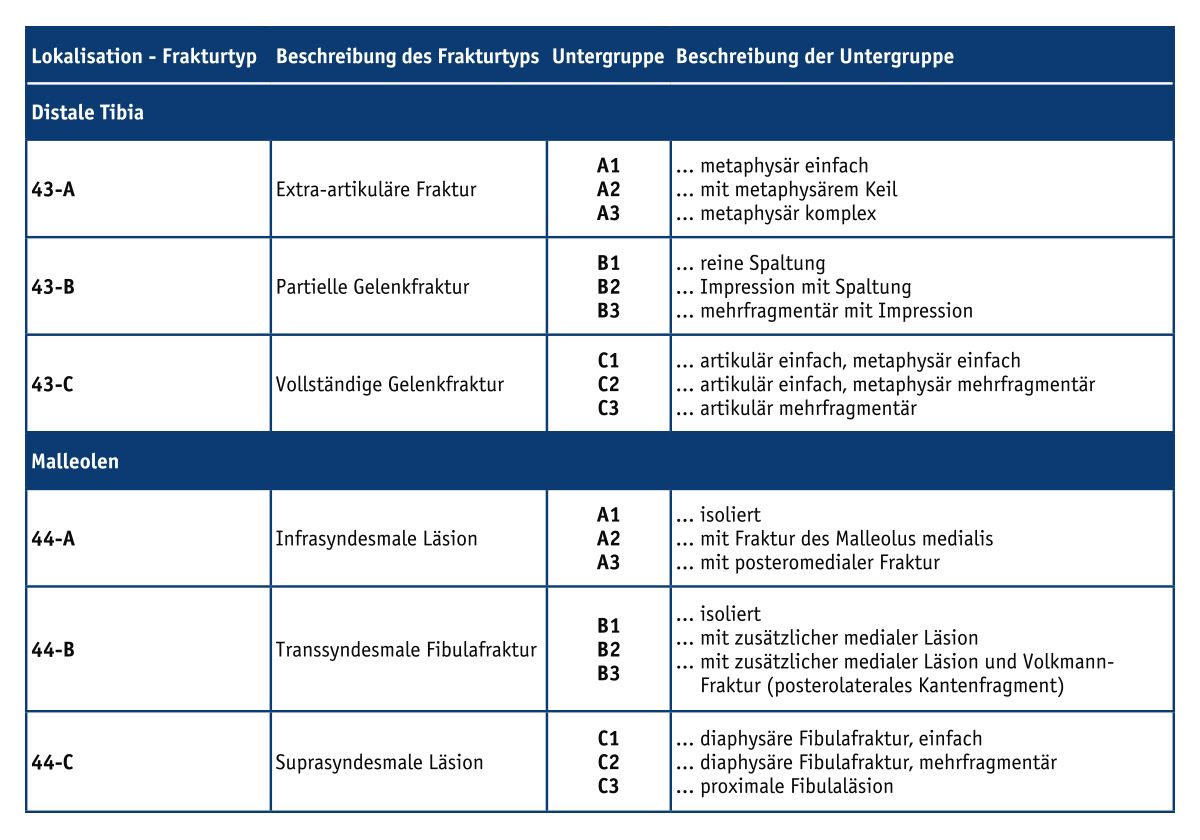
Es gibt verschiedene Möglichkeiten, nach denen Frakturen des Sprunggelenks eingeteilt werden können. Eines der ersten Modelle stammt von LAUGE-HANSEN (1948), der durch klinische Beobachtungen und experimentelle Untersuchungen einen Zusammenhang zwischen Frakturmechanismus und Frakturmorphologie herstellte. Obwohl die LAUGE-HANSEN Klassifikation eine große prognostische und therapeutische Relevanz hat, ist ihre Anwendung in der Praxis aufgrund der detaillierten Subgruppen recht aufwendig [4, 5]. Einfacher ist die Handhabung der pathologisch-anatomischen Fraktureinteilung mittels Röntgenbild nach DANIS (1949) und WEBER (1966). Hierbei wird, je nach Frakturhöhe der Fibula in Bezug auf die Syndesmosebänder, zwischen drei verschiedenen Frakturtypen unterschieden (A, B, C). Eine Ergänzung dazu stellt die AO-Klassifikation nach MÜLLER, NAZARIAN, KOCH und SCHATZKER (1990) dar. Sie erweitert die ABC-Einteilung um Untergruppen, die mit dem Schweregrad der Begleitverletzungen ansteigen (siehe Tab. 2) [6, 4].
Tab. 2: AO-Klassifikation (nach MÜLLER) der distalen Tibia und Fibula [modifiziert nach 7]
Frakturarten des Sprunggelenks
Malleolarfraktur
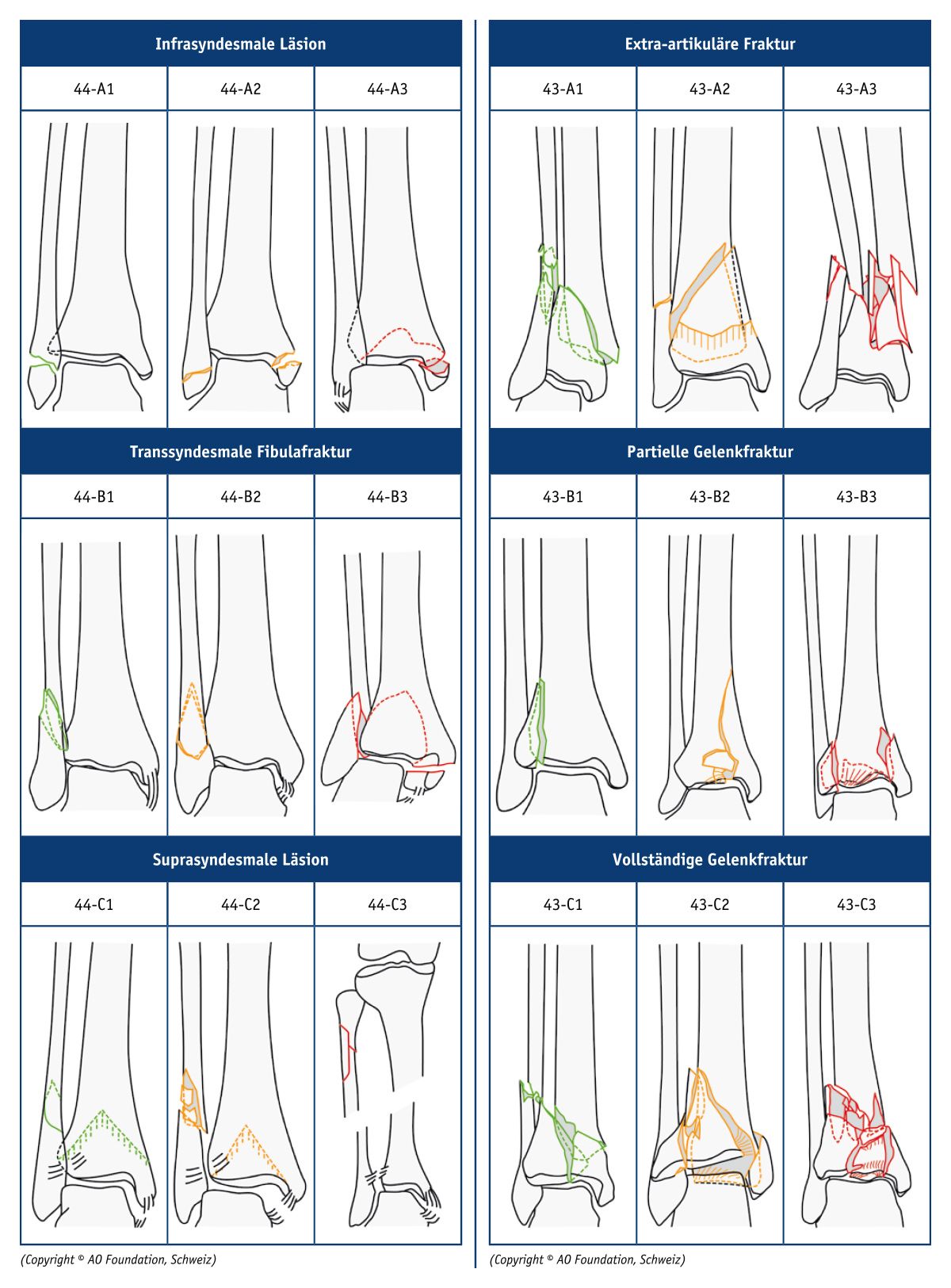
Die Malleolarfraktur bezeichnet den Bruch der distalen Fibula (Malleolus lateralis) in Höhe der proximalen oder distalen Syndesmose. Sie geht ohne oder mit Begleitverletzungen der Syndesmosebänder, des Malleolus medialis oder des medialen und lateralen Bandapparates einher. Ätiologisch sind Malleolarfrakturen meist auf eine Pronation oder Supination bei gleichzeitiger Eversion oder Inversion des Fußes durch indirekte Gewalteinwirkungen zurückzuführen [6]. Typische Risikosportarten, bei denen häufig Frakturen im Bereich der Malleolen auftreten, sind Fußball, Hallensportarten sowie Laufen (insbesondere Orientierungsläufe) [1]. Tabelle 3 veranschaulicht die Einteilung der Malleolarfrakturen nach der AO-Klassifikation anhand von Bildern.
Tibiafraktur
Eine Fraktur der distalen Tibia (Malleolus medialis) entsteht meist infolge einer größeren Gewalteinwirkung. Ursache einer solchen Stauchung ist z. B. ein Sturz aus großer Höhe. Darüber hinaus kann es zum Abbruch der Tibiahinterkante bei übermäßiger Dorsalextension mit Subluxation kommen. Umgekehrt ist unter außerordentlicher Plantarflexion mit Luxatio anterior der Abbruch der Tibiavorderkante möglich [2, 8]. Tibiafrakturen sind typische Skiverletzungen, die meist infolge eines Sturzes bei hoher Geschwindigkeit entstehen. Tabelle 4 veranschaulicht die Lokalisation und Morphologie möglicher distaler Tibiafrakturen klassifiziert nach der Arbeitsgemeinschaft für Osteosynthese (AO).
Talusfraktur
Die Talusfraktur ist in der Regel die Folge eines größeren Traumas und tritt nur selten bei sportlichen Aktivitäten auf. Typischer Pathomechanismus ist das Anstoßen des Talushalses bei forcierter Dorsalextension an die untere Tibiakante. Innerhalb der verschiedenen Sportarten ist das Risiko für Talusfrakturen beim Gleitschirmfliegen, Klettern und Hochspringen besonders hoch. Darüber hinaus treten Frakturen des Sprungbeins häufig bei Fußballern, alpinen Skiläufern, Skispringern, Hochspringern und Hallensportlern auf. Eine besondere Form der Talusfraktur ist der sogenannte „Snowboarder´s Ankle“, die vorwiegend bei Snowboardern auftritt und mit einem Abriss des Processus lateralis tali einhergeht. In der Akutdiagnostik können Frakturen des Talus leicht mit einer lateralen Sprunggelenksdistorsion verwechselt werden [Knupp und Hintermann 2006]. Die Talusfrakturen werden nach MARTY und WEBER in 5 Typen klassifiziert: periphere Frakturen (Typ I), nicht-dislozierte Korpus- und proximale Kollumfrakturen (Typ II), dislozierte zentrale Frakturen (Typ III) und Trümmerfrakturen (Typ IV) [9].
Calcaneusfraktur
Eine Fraktur des Calcaneus entsteht bei direkter Krafteinwirkung auf die Ferse, so z. B. bei einem Sturz aus großer Höhe mit Landung auf den Fersen. Aufgrund häufiger Begleitverletzungen sollten diagnostizierte Calcaneusfrakturen nicht nur mittels Röntgenbild, sondern zusätzlich durch eine Computertomographie (CT) analysiert werden, um das Ausmaß der Verletzung genau abschätzen und ein geeignetes Therapieschema erstellen zu können. Abrissfrakturen des Processus anterior calcanei können leicht übersehen werden und verursachen persistierende Schmerzen im Mittelfußbereich. Zu den Sportarten, die mit einem erhöhten Risiko für Frakturen des Calcaneus verbunden sind, gehören vor allem das Fallschirmspringen und Gleitschirmfliegen, aber auch das Klettern. Das Risiko für Calcaneusfrakturen mit gleichzeitigem Abriss des Processus anterior calcanei infolge eines Inversions-/Adduktionstraumas ist bei Orientierungsläufern, Fußball- und Rugbyspielern besonders hoch [1].
Stressfraktur
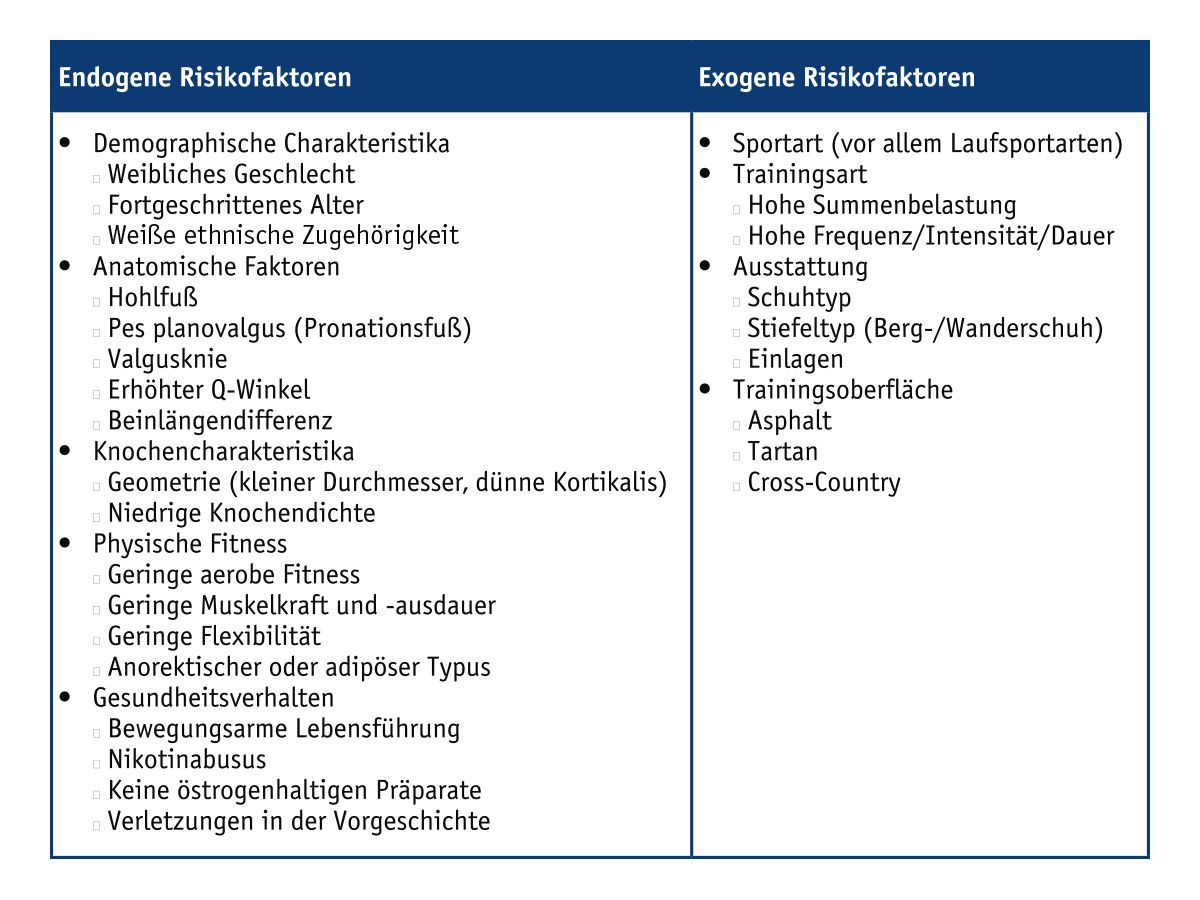
Stressfrakturen – auch Ermüdungs- oder Marschfrakturen genannt – treten auf, wenn die Belastung eines Knochenabschnittes größer ist als seine mechanische und biologische Belastbarkeit und somit ein Missverhältnis zwischen Belastung und Belastbarkeit besteht. Liegt eine Mehrbelastung vor, werden Umbaureaktionen ausgelöst, mit denen der Knochen versucht sich an die fortwährende Überlastung anzupassen. Dabei entsteht ein Ungleichgewicht zwischen der Aktivitätsrate der Osteoblasten und Osteoklasten. Übersteigt zum Beginn des Knochenumbaus die Osteoklastenaktivität die der Osteoblasten, kommt es bei anhaltender Belastung zu Stressfrakturen. Grundsätzlich wird die Entstehung von Ermüdungsfrakturen durch verschiedene endogene und exogene Risikofaktoren gefördert (siehe Tab. 5) [10, 2].
Bezogen auf die Gesamtheit an Sportverletzungen treten Stressfrakturen nur mit einer Inzidenz von 1 bis 2 % auf. Allerdings zeigt sich auch hier ein sportartenabhängiges Risiko. So sind bei Leichtathleten immerhin 15 bis 20 % aller Verletzungen auf Stressfrakturen zurückzuführen [12]. Etwa 70 % der insgesamt auftretenden Ermüdungsfrakturen werden bei Läufern diagnostiziert [10].
Am häufigsten treten Stressfrakturen in den unteren Extremitäten und dort insbesondere in der Tibia auf. Die Klassifikation erfolgt in Abhängigkeit von der jeweiligenLokalisation und unterscheidet zwischen den Hochrisiko- und Niedrigrisiko-Stressfrakturen. Letztere zeigen einen insgesamt guten Heilungsverlauf. Zudem weisen sie bezüglichAchsenfehler, Pseudoarthrosen und verzögertem Heilungsprozess eine geringere Komplikationsrate auf als Hochrisiko-Stressfrakturen, die oft deutlich langsamer verheilen.
Beispiele für Frakturen aus der Hochrisikogruppe betreffen die ventrale Tibiakante, den Malleolus medialis oder das Os naviculare [10, 11].
Tab. 3 (links): Klassifikation der Malleolarfrakturen nach der Müller-AO-Frakturklassifikation, Tab. 4 (rechts): Klassifikation der distalen Tibiafrakturen nach der Müller-AO-Frakturklassifikation
Tab. 5: Endogene und exogene Risikofaktoren für Stressfrakturen [modifiziert nach 10]
Therapie von Sprunggelenksfrakturen
Ein wichtiges Ziel in der Behandlung von Sprunggelenksfrakturen ist die exakte anatomische Rekonstruktion, um die Entwicklung einer Arthrose infolge einer Inkongruenz der Gelenkflächen und/oder einer Stufenbildung innerhalb der Gelenkfläche zu vermeiden. Die Rekonstruktion sollte dabei stets mit der Retention des verletzten Gelenks bis zur Frakturheilung einhergehen. Gleichzeitig sollten bestehende Schmerzen beseitigt oder zumindest reduziert werden. Ziel ist die Wiederherstellung der Gelenkbeweglichkeit und Funktion [6].
Je nach Schweregrad der vorliegenden Fraktur kann die Behandlung einer Sprunggelenksverletzung mittels konservativer oder operativer Therapie erfolgen. Eine konservative Therapie ist beispielsweise bei nicht-dislozierten Frakturen vom Typ A oder B (nach WEBER) indiziert. Eine operative Behandlung ist hingegen angezeigt, wenn die Sprunggelenksfraktur z. B. mit einer Dislokation einhergeht.
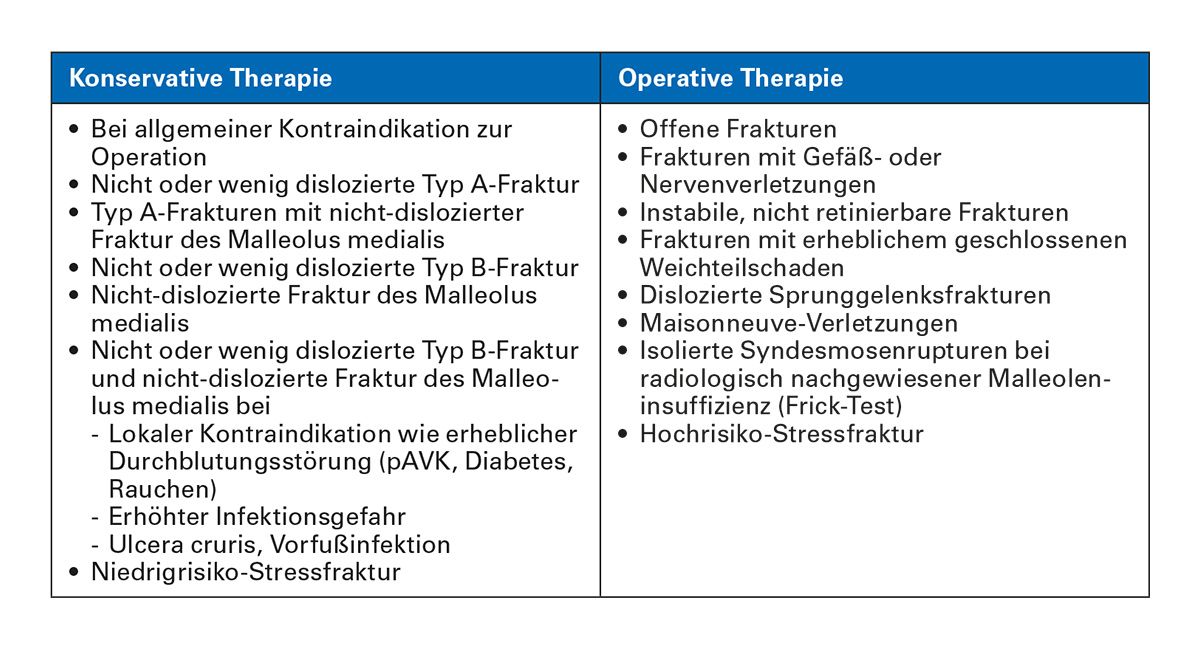
Tabelle 6 gibt einen Überblick über die verschiedenen Indikationen zur konservativen bzw. operativen Behandlung. Unabhängig von der Wahl des Therapieschemas wird ein möglichst unmittelbarer Behandlungsbeginn empfohlen [6].
Tab. 6: Indikationen der konservativen und operativen Therapie [modifiziert nach 6]
Konservative Therapie
Zu Beginn einer konservativen Therapie steht die Beratung des Patienten, der über seine Verletzung, deren Verlauf sowie die Vor- und Nachteile der gewählten Therapie aufgeklärt werden muss. Zudem sollte er Informationen zu bestehenden Alternativverfahren erhalten. Meist beginnt die konservative Therapie mit der Reposition dislozierter Frakturen. Anschließend wird die verletzte Gelenkregion für etwa 6 Wochen ruhiggestellt. Alternativ ist auch bei stabilen Verhältnissen eine funktionelle Behandlung unter Verwendung von beispielsweise Orthesen möglich. Parallel zur Retention erfolgen eine medikamentöse Thromboseprophylaxe sowie gegebenenfalls die Gabe nicht-steroidaler Antirheumatika zur entzündungshemmenden Schmerzbehandlung. Zudem sollte der Patient zu selbständigen Mobilisationsübungen angehalten werden, die nach Ende der Retention durch eine individuelle Physiotherapie ergänzt werden können [6].
Operative Therapie
Das Ziel einer operativen Behandlung ist neben der exakten anatomischen Reposition und Retention des frakturierten Gelenks die frühfunktionelle Nachbehandlung.
Der Zeitpunkt der Operation ist abhängig von der jeweiligen Verletzungssituation. So gibt es einzelne Umstände, die eine sofortige Operation bedingen. Hierzu zählen offene Frakturen, Frakturen mit fortbestehender Subluxation/Luxation sowie Frakturen mit schwerem geschlossenen Weichteilschaden (z. B. Spannungsblasen). Grundsätzlich ist eine Operation jedoch solange möglich, wie es die Weichteilschwellungen zulassen. Sind diese bereits zu weit fortgeschritten, muss der Eingriff verschoben werden bis die Weichteile wieder abgeschwollen sind. Im Rahmen der Operation stehen dem Chirurgen unterschiedliche Verfahren zur Verfügung.
Neben der Behandlung der ossären Frakturbestandteile werden auch die Begleitverletzungen umliegender Weichteile versorgt. Neben der Weiterführung der Thromboseprophylaxe, bei offenen Frakturen gegebenenfalls der Antibiotikatherapie, sind die Physiotherapie, abschwellende Maßnahmen und eine Frühmobilisation mit Belastungsaufbau Bestandteile der postoperativen Behandlung [6].
Bandverletzungen des Sprunggelenks
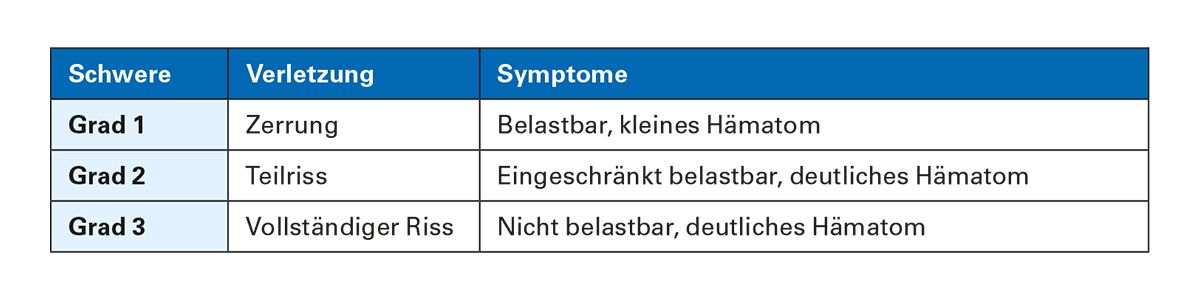
Bandverletzungen sind die häufigsten Verletzungen im Sport. Sie gehen meist mit Hämatomen und einer Druckschmerzhaftigkeit entlang des geschädigten Ligaments einher. Zur Klassifikation eignet sich die Einteilung in drei Schweregrade nach der „American Medical Association“, wobei insbesondere zwischen Grad I und II nicht immer sicher differenziert werden kann. Oft ist jedoch eine Zuteilung anhand vorliegender Symptome möglich, die mit dem Ausmaß der Verletzung korrelieren (siehe Tab. 7).
Tab. 7: Klassifikation von Bandverletzungen nach der „American Medical Association“ [modifiziert nach https://ama-guides.ama-assn.org/]
Verletzungen der einzelnen Bandapparate
Verletzungen des lateralen Bandapparates
Der laterale Bandapparat des Sprunggelenks umfasst die Ligg. talofibulare anterius und posterius sowie das Lig. calcaneofibulare (siehe Modul 1, Tab. 1). Eine Ruptur der Außenbänder entsteht typischerweise dann, wenn das obere Sprunggelenk über seine eigentliche Beweglichkeit hinaus in Supinations- und Inversionsstellung des Fußes bewegt wird. Folge einer solchen Krafteinwirkung ist die partielle oder komplette Ruptur des lateralen Bandapparates.
Darüber hinaus gehende mögliche Begleitverletzungen sind die Ruptur der Sprunggelenkskapsel, osteochondrale Frakturen oder eine Ruptur der Syndesmosebänder. Im Rahmen des Pathomechanismus rupturiert zunächst das Lig. talofibulare anterius, gefolgt von einer partiellen oder vollständigen Ruptur des Lig. calcaneofibulare. Das posteriore Lig. talofibulare ist nur selten betroffen und spielt bei lateralen Bandverletzungen nur eine untergeordnete Rolle [12, 5].
Zur Diagnose einer Außenbandruptur eignet sich im Rahmen der klinischen Untersuchung der vordere Schubladen-Test sowie der Talar Tilt Test 1 (siehe Modul 1, Tab. 4). So deutet ein pathologischer Befund im vorderen Schubladen-Test auf eine Ruptur des Lig. talofibulare anterius, ein positives Ergebnis des Talar Tilt Tests 1 auf ein rupturiertes Lig. calcaneofibulare hin [12, 5].
Verletzungen des medialen Bandapparates
Der mediale Bandapparat umfasst das Lig. deltoideum, das aus einem oberflächlichen und einem tiefen Anteil besteht (siehe Modul 1). Da das mediale Kollateralband in
seiner Gesamtheit sehr kräftig und stabil ist, rupturiert es meist erst infolge schwerwiegender Verletzungen, die mit Frakturen einhergehen. Als typischer Pathomechanismus gilt die Eversionsbewegung, bei der die Talusgelenkfläche an den Malleolus lateralis stößt. Es kommt zur Distorsion und gegebenenfalls zur partiellen oder vollständigen Ruptur des Lig. deltoideum. Gleichzeitig ist eine Verletzung der Syndesmosebänder möglich. Vor diesem Hintergrund ist bei Röntgenbildaufnahmen auf den Abstand zwischen Malleolus medialis und Talus zu achten, der im Seitenvergleich bei vorliegender Bandruptur deutlich vergrößert ist. Zur klinischen Verdachtsuntersuchung eignet sich der Talar Tilt Test 2, der bei einem pathologischen Befund auf eine Ruptur des Lig. deltoideum hinweist [12, 8].
Verletzungen der Syndesmosebänder
Der Bandapparat der Syndesmose umfasst die Ligg. tibiofibulare anterius und posterius. Häufig wird auch die Membrana interossea den Syndesmosebändern zugeordnet, da sie das Bindeglied zwischen Tibia und Fibula darstellt und an der Stabilität der Malleolengabel maßgeblich beteiligt ist (siehe Modul 1). Zur Ruptur der Syndesmosebänder kommt es meist infolge einer Supinations- und/oder Eversionsbewegung. Als erstes rupturiert dabei das Lig. tibiofibulare anterius, mit anschließender Ruptur der Membrana interossea. Zuletzt reißt auch das Lig. tibiofibulare posterius. Hält die starke Krafteinwirkung weiter an, so kann die Fibula oberhalb der Syndesmose frakturieren.
In diesem Fall reicht die Ruptur der Membrana interossea bis auf Höhe der Fraktur. Eine isolierte Verletzung der Syndesmosebänder ohne ossäre Begleitverletzungen ist eine eher seltene Sportverletzung, die mit einer Inzidenz von 1 bis 11 % vorkommt.
Mit Hilfe von Funktionstests kann der Verdacht auf eine Syndesomoseverletzung bestärkt werden. Hierzu eignet sich beispielsweise der Kleiger-(Außenrotationsstress-)Test (siehe Modul 1, Tab. 4). Treten während des Testverlaufs Schmerzen im ventrolateralen oberen Sprunggelenk auf, deutet dies auf eine Verletzung der Syndesmosebänder hin. Häufig sind die Schmerzen auch mit einer Verletzung des Lig. deltoidem verbunden [12, 13, 14].
Therapie von Bandverletzungen
Das Grundprinzip in der konservativen Therapie von Bandverletzungen ist die sogenannte RICE-(rest, ice, compression, elevation) Methode, die unabhängig vom Verletzungsgrad (I bis III) angewandt wird. Obwohl das RICE-Prinzip seit 1978 fest etabliert ist, wird es in der modernen Sportorthopädie zunehmend durch erweiterte Protokolle wie POLICE (Protection, Optimal Loading, Ice, Compression, Elevation) oder PEACE and LOVE ersetzt [15].
Diese erweiterten Konzepte betonen vor allem die Wichtigkeit der frühzeitigen, adaptierten Belastung (Optimal Loading bzw. Load, Exercise), um die Gewebeheilung zu stimulieren und langfristige Funktionseinschränkungen zu vermeiden. Unabhängig davon bleibt RICE eine einfache und effektive Sofortmaßnahme zur Erstversorgung akuter Bandverletzungen [15]. Die initiale Therapie gem. dem RICE-Schema („rest, ice, compression and elevation“) kann durch zusätzliche Physiotherapie hinsichtlich Schmerzreduktion, Abschwellung und Funktion ergänzt werden [16].
Eine stabile Zerrung kann mit elastischer Bandage für einige Tage, die Bandruptur mit einer Orthese für 5-6 Wochen erfolgreich behandelt werden. Eine propriozeptive Nachbehandlung ist die beste Prophylaxe von Rezidiv-Traumata [17]. Die funktionelle Therapie wird meist mit semirigider / rigider Orthese für 5-6 Wochen eingeleitet, die gegenüber elastischer Bandage oder dem Tape-Verband zu weniger Schwellung, zur kürzeren Krankheitsdauer und zu weniger Hautproblemen führt [17].
Grundsätzlich umfasst die frühfunktionelle Therapie neben dem Gelenkschutz den individuellen Belastungsaufbau durch physiotherapeutische Maßnahmen und die Wiederaufnahme von sportlichen Aktivitäten, denn im Rahmen der Therapie von Gelenkverletzungen ist es wichtig, die Stabilität des Gelenks wiederherzustellen. Eine Möglichkeit stellt die Anwendung von orthopädietechnischen Stabilisierungshilfen wie Bandagen oder Orthesen dar [18]. So verzögern Bandagen beispielsweise die Umknickbewegung und nehmen damit Einfluss auf die Zeit, die der Muskulatur zwischen Stimulus (Unfall) und Aktionspotenzial (Muskelkontraktion) bleibt.
Zudem stimulieren Bandagen durch den stetigen engen Kontakt zum Gelenk und der umliegenden Haut die dort vorhandenen propriozeptiven Rezeptoren, wodurch die Stabilität des Gelenks zunimmt. Durch die passgenaue Form und das enge Anliegen einer Bandage wird darüber hinaus das subjektive Instabilitätsgefühl, das bisherigen Untersuchungen zufolge der wichtigste Faktor für ein erhöhtes Verletzungsrisiko ist, deutlich verbessert [19, 18, 20].
Je nach Ausmaß und Art der Verletzung kann auch eine kurzzeitige Ruhigstellung des Sprunggelenks mit Hilfe einer Schiene notwendig sein. Dies ist beispielsweise bei Syndesmoseverletzungen dritten Grades der Fall [12, 21].
Alle weiteren, darüber hinaus gehenden Behandlungsmaßnahmen sind immer individuell in Abhängigkeit von der vorliegenden Verletzung zu verordnen. Notwendig ist bei entsprechender Indikation eine medikamentöse Therapie zur Schmerzbehandlung oder Thromboseprophylaxe. Auch weitere Hilfsmittel, beispielsweise ein Kompressionsstrumpf, können sinnvoll sein.
Neben der konservativen Therapie gibt es auch im Rahmen von schweren Bandverletzungen im Einzelfall die Möglichkeit der operativen Versorgung. Das Ziel der operativen Therapie ist es, die rupturierten Bänder durch eine Naht wiederherzustellen. Die meisten akuten Bandläsionen werden jedoch konservativ behandelt, da der hierdurch erzielte Erfolg hinsichtlich der Sprunggelenksstabilität mit dem einer operativen Therapie vergleichbar ist. Dies gilt insbesondere für Verletzungen der Schweregrade I und II. Die Behandlung von Bandläsionen dritten Grades wird zum Teil noch kontrovers diskutiert, allerdings scheint eine Operation z. B. bei Sportlern, deren Aktivität eine hohe Stabilität im Sprunggelenk bedarf, bei Begleitverletzungen oder bei Patienten, die eine chronische Instabilität entwickeln, möglich. Postoperativ ist ebenfalls eine frühfunktionelle Therapie durch orthopädietechnische Mittel wie Orthesen oder Bandagen und eine frühzeitige Mobilisierung wichtig [22, 21].
Knorpelschaden im oberen Sprunggelenk
Ein Knorpelschaden im oberen Sprunggelenk beschreibt eine degenerative oder traumatische Schädigung des Gelenkknorpels, der die Gelenkflächen von Talus (Sprungbein) und Tibia (Schienbein) überzieht. Dieser hyaline Knorpel ermöglicht eine nahezu reibungsfreie Bewegung und wirkt stoßdämpfend. Ein Knorpeldefekt kann von oberflächlichen Weichteilschäden bis hin zu tiefgreifenden Defekten mit Exposition des subchondralen Knochens reichen (z. B. bei einer Osteochondrosis dissecans).
In fortgeschrittenen Fällen kann sich eine sekundäre Arthrose des Sprunggelenks entwickeln. Die Klassifikation erfolgt häufig nach Outerbridge oder ICRS, wobei insbesondere bei osteochondralen Läsionen eine Differenzierung zwischen rein knorpelären und knorpel-knochigen Defekten von klinischer Relevanz ist [23].
Klassifikationen von Knorpelschaden
Klassifikation nach Outerbridge
Die Outerbridge-Klassifikation (23-25) wurde ursprünglich für das retropatellare Knorpelgewebe des Knies entwickelt, findet aber auch in der Diagnostik des oberen Sprunggelenks Anwendung. Sie basiert auf dem makroskopischen Bild, typischerweise bei arthroskopischer Begutachtung.
Tab. 8: Outerbridge-Klassifikation (23-25)
ICRS-Klassifikation (International Cartilage Repair Society)
Die ICRS-Klassifikation [26] erlaubt eine differenziertere Einteilung, insbesondere im Rahmen der präoperativen MRT(Magnetresonanztomographie)-Befundung oder intraoperativ bei arthroskopischen Eingriffen. Sie eignet sich zur Standardisierung von Studien und OP-Dokumentationen und berücksichtigt sowohl die Tiefe als auch die Morphologie der Läsion.
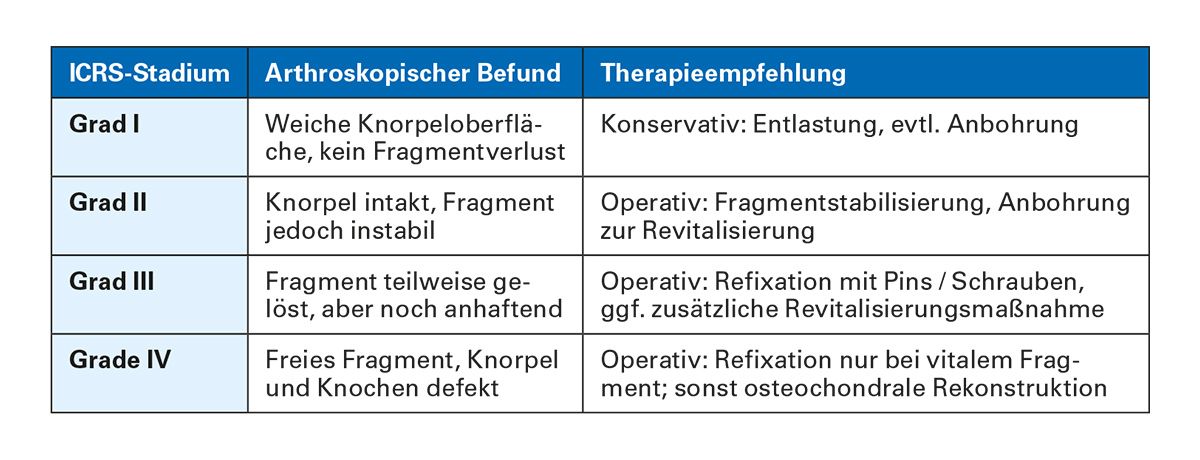
Tab. 9: ICRS-Klassifikation [26]
Vergleich und klinische Relevanz
Beide Klassifikationen sind in der Praxis weit verbreitet. Die Outerbridge-Klassifikation wird häufiger bei arthroskopischen Eingriffen verwendet, während die ICRS-Klassifikation auch in der präoperativen Bildgebung (z. B. MRT-Befundung) eingesetzt wird. Die genaue Graduierung hat direkte therapeutische Implikationen – z. B. konservative Maßnahmen bei Grad I-II, operative Rekonstruktionen oder regenerative Verfahren bei Grad III-IV.
Epidemiologie
Knorpelschäden im oberen Sprunggelenk sind seltener als im Knie oder in der Hüfte [27]. Weltweit sind etwa 1 % der adulten Bevölkerung betroffen [28]. Die Inzidenz talarer OLT-Läsionen (Osteochondrale Läsion des Talus) nach einer Knöcheldistorsion wird mit bis zu 6,5 % angegeben. Fast allen diesen Läsionen ging ein Trauma (Verstauchung oder Fraktur) voraus [29]. Männer sind häufiger betroffen, insbesondere bei traumatischer Genese [29].
Pathogenese
Die Pathogenese ist multifaktoriell (Tab. 10) und umfasst sowohl akute als auch chronische Ursachen Die wesentlichen pathogenetischen Faktoren der posttraumatischen OSG-Arthrose sind Instabilität, Inkongruenz der Gelenkflächen und Knorpelschäden [27, 28, 30]. Am häufigsten entstehen Knorpeldefekte im OSG infolge eines Supinationstraumas mit begleitender Bandinstabilität. Dabei führen Scher- oder Kompressionskräfte zu mechanischer Schädigung des Knorpelgewebes. Wiederholte Mikrotraumatisierung, insbesondere bei Leistungssportlern, kann die Knorpelhomöostase stören und degenerative Prozesse begünstigen. In bestimmten Fällen kommt es zur Ausbildung osteochondraler Läsionen, etwa infolge subchondraler Osteonekrose, wie sie bei der Osteochondrosis dissecans beobachtet wird. Chronische Instabilität, Achsfehlstellungen sowie metabolische Faktoren tragen zusätzlich zur Progression der Knorpeldegeneration bei.
Tab. 10: Multifaktorielle Pathogenese von Knorpelschäden im OSG
Risikofaktoren
Risikofaktoren für die Entwicklung eines Knorpelschadens am OSG [28, 31] sind
- Verletzungen: insbesondere Supinationstraumen
- Chronische Bandinstabilität
- Achsenfehlstellungen (z. B. Varus-/Valgusdeformität)
- Übergewicht (führt zu höherer Gelenkbelastung)
- Voroperationen oder intraartikuläre Frakturen
- Knorpelschäden des Sprunggelenks
Eine exakte Analyse der individuellen Belastungssituation ist für die therapeutische Entscheidungsfindung essenziell.
Symptome
Klinisch äußert sich ein Knorpelschaden im OSG zunächst meist durch belastungsabhängige Schmerzen im Bereich des Sprunggelenks, insbesondere bei längerer Gehstrecke, Bergabgehen oder sportlicher Aktivität. Im Verlauf können sich die Beschwerden auf Alltagsbelastungen ausweiten, teils bestehen auch Ruheschmerzen. Schwellungsneigung, Bewegungseinschränkungen sowie ein subjektives Instabilitätsgefühl sind häufige Begleitphänomene. Bei osteochondralen Fragmenten kann es zu Blockierungen und akuten Gelenkverriegelungen kommen. Ein Knorpelschaden im OSG kann sich schleichend oder akut bemerkbar machen.
Therapie
Therapeutisch richtet sich das Vorgehen nach dem Schweregrad der Läsion, der Symptomatik sowie dem Aktivitätsprofil des Patienten.
Konservative Therapie
Bei geringer Ausprägung und stabiler Gelenksituation steht die konservative Therapie im Vordergrund. Diese umfasst physiotherapeutische Maßnahmen zur Verbesserung von Propriozeption und muskulärer Führung, Entlastung durch Orthesen/Bandagen sowie medikamentöse Schmerztherapie mittels NSAR. Injektionsbasierte Verfahren mit Hyaluronsäure oder plättchenreichem Plasma (PRP) können erwogen werden [31, 32].
Konservative Therapiemöglichkeiten
- Physiotherapie: Verbesserung der Gelenkstabilität, Muskelkräftigung
- Bandagen, Orthesen: zur Entlastung und Stabilisierung. Ggf. Orthopädischer Schuh, orthopädische Schuhzurichtung
- NSAR zur Schmerz- und Entzündungshemmung
- Injektionen: z. B. Hyaluronsäure oder PRP (plättchenreiches Plasma) [33, 34]
Operative Therapie
Bei persistierender Symptomatik oder höhergradigen Knorpelschäden ist eine operative Intervention angezeigt. Arthroskopische Verfahren wie Débridement oder Mikrofrakturierung kommen bei kleineren Defekten zur Anwendung. Größere Defekte erfordern oft rekonstruktive Verfahren wie die osteochondrale Transplantation (OATS), die autologe Matrix-induzierte Chondrogenese (AMIC) oder in ausgewählten Fällen die autologe Chondrozytentransplantation (ACT). Bei ausgeprägten biomechanischen Fehlstellungen sollte eine begleitende Korrekturosteotomie in Erwägung gezogen werden. In Endstadien mit ausgedehnter Gelenkdestruktion kann ein endoprothetischer Gelenkersatz oder eine Arthrodese erforderlich sein. Operative Therapiemöglichkeiten wurden in jüngerer Literatur eingehend beschrieben [35-40].
Operative Therapiemöglichkeiten
- Arthroskopische Débridement: Glättung Knorpelflächen
- Mikrofrakturierung / Pridie-Bohrung: Stimulation der Knorpelregeneration
- OATS / Mosaikplastik: Knorpel-Knochen-Transplantation
- AMIC-Technik (Autologe Matrix-induzierte Chondrogenese)
- Autologe Chondrozyten-Transplantation (ACT) [41]
- Korrekturosteotomien: bei Achsfehlstellungen
- Endoprothetischer Gelenkersatz: als ultima ratio bei fortgeschrittener Arthrose
- Arthrodese als Alternative zur Prothese bei schwerer Therapie resistenter Arthrose
Osteochondrosis dissecans
Osteochondrosis dissecans tritt am häufigsten bei aktiven Kindern, Jugendlichen und jungen Erwachsenen auf. Besonders häufig betroffen sind das Knie, der Ellenbogen oder das Sprunggelenk. Unterschieden wird eine juvenile und eine adulte Form [42]. Die juvenile Form bezeichnet das Auftreten bei offenen Wachstumsfugen, die adulte Form das Auftreten bei geschlossenen Wachstumsfugen [43].
Verschiedene ätiopathogenetische Theorien werden berichtet. Dazu gehören lokale Ischämie, abnorme enchondrale Ossifikation der sekundären subartikulären Epiphyse, wiederholte Mikrotraumata, vaskuläre Störungen sowie eine genetische Prädisposition. Die Ätiologie ist multifaktoriell. Dabei stellt die Osteochondrosis dissecans eine umschriebene, ischämisch bedingte subchondrale Osteonekrose dar, die in weiterer Folge zur Ablösung eines osteochondralen Fragments führen kann. Sie tritt bevorzugt im Bereich mechanisch belasteter Gelenkregionen auf, wobei das Kniegelenk – insbesondere die mediale Femurkondyle – am häufigsten betroffen ist [42, 44].
Klassifikationen der Osteochondrosis dissecans
Die Klassifikationen (Tab. 11, 12) dienen der objektiven Einschätzung des Läsionsstadiums und sind entscheidend für die Auswahl des individuellen Therapiekonzepts. In der Praxis erfolgt die Zuordnung häufig kombiniert (radiologisch vorab, intraoperativ arthroskopisch bestätigt).
Tab. 11: Bruns-Klassifikation [45, 46]
Tab. 12: ICRS-Klassifikation (arthroskopisch) [47, 48]
Therapie
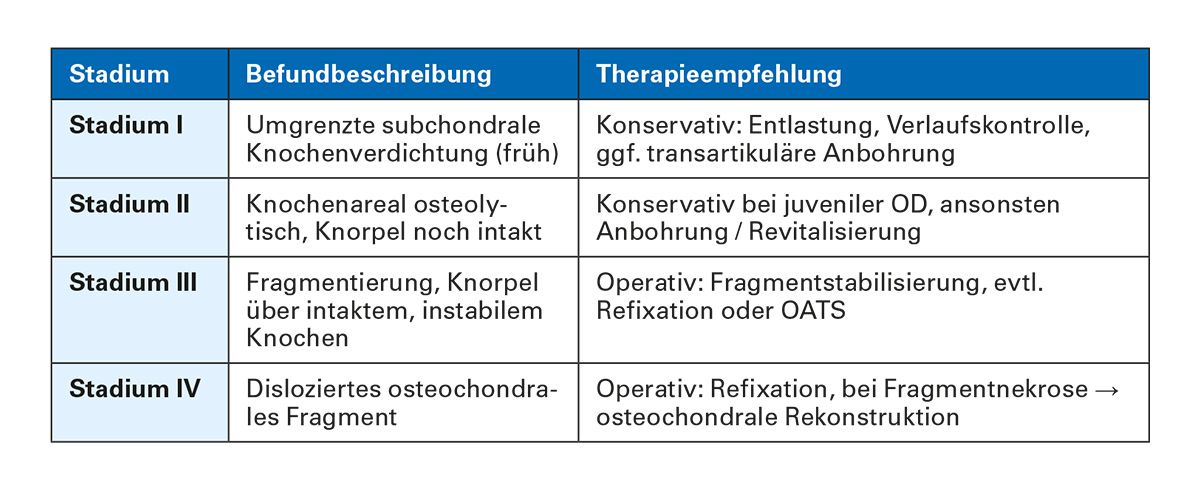
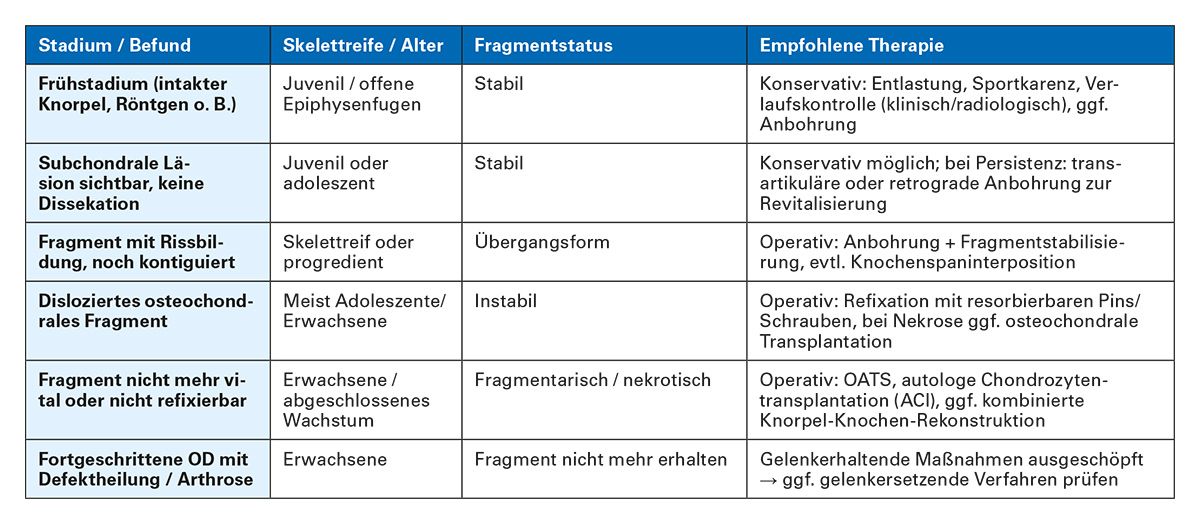
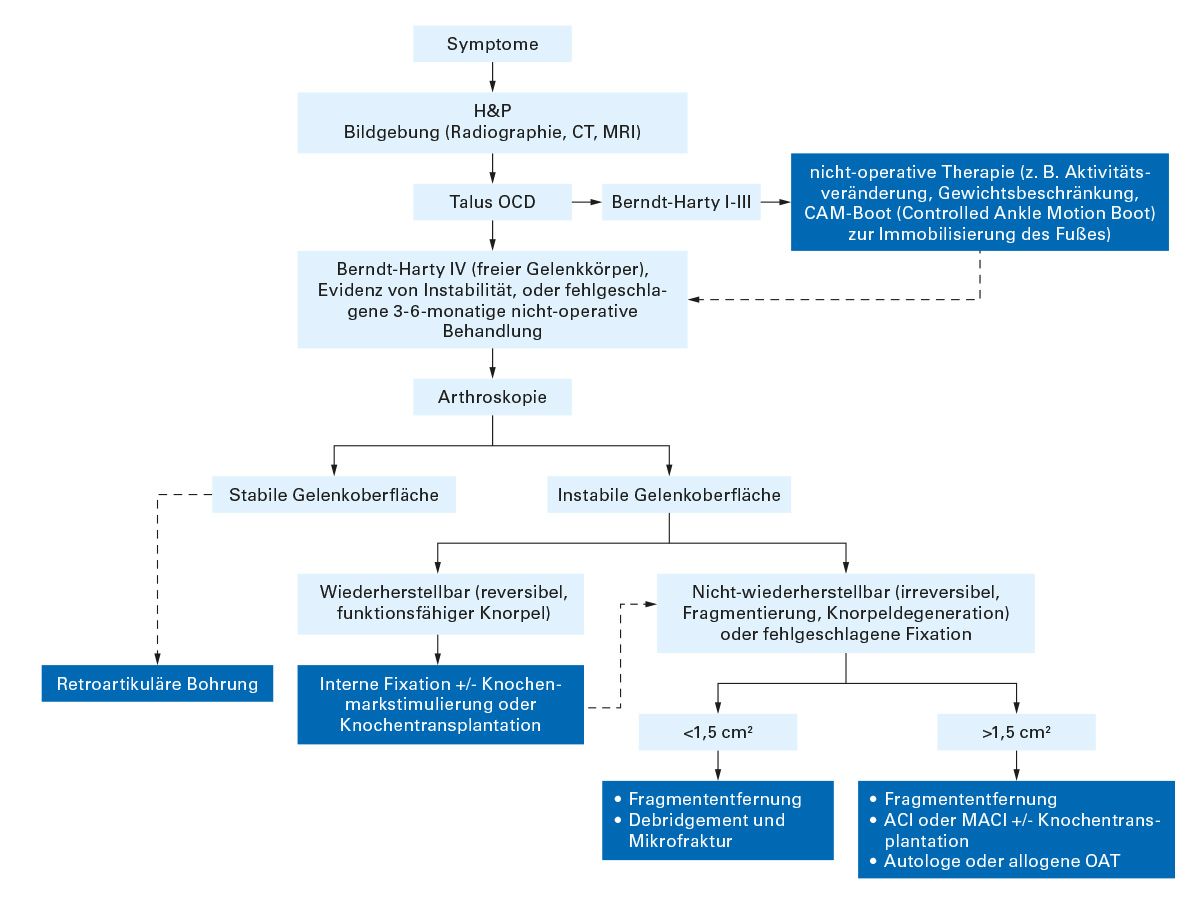
Die Therapie richtet sich primär nach dem Alter des Patienten, dem radiologischen/ kernspintomographischen Stadium der Läsion sowie der Fragmentstabilität [49-52], (Tab. 13, Abb. 1).
Konservative Therapie
In frühen, stabilen Stadien bei skelettal noch nicht ausgereiften Patienten ist ein konservatives Vorgehen indiziert. Dieses umfasst
- die Entlastung des betroffenen Gelenks, ggf. unter Verwendung von Unterarmgehstützen über 6-12 Wochen,
- die Einschränkung sportlicher Aktivitäten insbesondere für sportartspezifische Belastungen wie Laufen, Springen oder Richtungswechsel,
- eine physiotherapeutische gelenkschonende Mobilisation: zur Vermeidung von Muskelatrophie und Bewegungseinschränkungen
- sowie eine engmaschige klinisch-radiologische (ggf. kernspintomographische Verlaufskontrolle über mehrere Monate.
Operative Therapie
Bei ausbleibender Besserung, radiologischer Progredienz oder bei Nachweis einer Instabilität des Fragments ist eine operative Intervention indiziert. Ziel der operativen Therapie ist die Wiederherstellung der Gelenkfunktion und -integrität unter Erhalt der Knorpelstruktur.
Indikationen zur operativen Versorgung sind Versagen konservativer Maßnahmen, Fragmentinstabilität oder Dislokation, fortgeschrittene Stadien (Bruns III/IV oder ICRS III/IV) oder adulte Patienten mit geschlossener Epiphysenfuge [53]. Je nach Stadium und Fragmentbeschaffenheit kommen unterschiedliche, operative Verfahren zur Anwendung:
- Transartikuläre oder retrograde Anbohrung („drilling“): zur Stimulation der Reossifikation in Frühstadien ohne Fragmentablösung [54]
- Fixation instabiler oder teilabgelöster Fragmente mittels resorbierbarer Pins, Schrauben oder Fibrinkleber.
Bei fortgeschrittener OD mit Knorpeldefekten können Knorpel-Knochen-Kombinationseingriffe oder alternative rekonstruktive Maßnahmen herangezogen werden:
- Knochenspaninterposition, Osteochondrale autologe Transplantation (OATS): bei avitalen oder nicht-refixierbaren Fragmenten, Transplantation von osteochondralen Zylindern meist aus weniger belasteten Arealen des gleichen Gelenks
- Autologe Chondrozytenimplantation (ACI): bei größeren Knorpeldefekten ohne ausreichende Knochensubstanz
- Mosaikplastik oder kombinierte Knorpel-Knochen-Rekonstruktionen bei ausgedehnten Defekten
- Bei fortgeschrittener OD mit Knorpeldefekten: Knorpel-Knochen-Kombinationseingriffe oder alternative rekonstruktive Maßnahmen [52, 55, 56]
Die postoperative Nachbehandlung orientiert sich am jeweiligen Eingriff und umfasst in der Regel eine Phase der Teilbelastung, eine strukturierte physiotherapeutische Mobilisation sowie ggf. den Einsatz einer Motorschiene (CPM, Continuous Passive Motion). Langfristig ist eine sportartspezifische Belastungsanpassung zu empfehlen, um eine Überlastung des betroffenen Gelenks zu vermeiden.
Postoperative Nachbehandlung der Osteochondrosis dissecans
- Gelenkentlastung für 6-12 Wochen je nach Verfahren
- Frühfunktionelle Mobilisation
- Physiotherapie zur Koordinations- und Muskelkräftigung
- Langfristige Belastungssteuerung mit schrittweiser Rückführung in sportliche Aktivität unter funktioneller Kontrolle
Das Ziel aller Therapieansätze ist der Erhalt einer glatten, belastbaren Gelenkfläche, um eine langfristige Arthroseentwicklung zu verhindern und die volle Belastungsfähigkeit des Gelenks wiederherzustellen.
Tab. 13: Therapieoptionen bei Osteochondrosis dissecans – Übersicht nach Stadium [57, 58, 59]
Abb. 1: Allgemeiner Behandlungsalgorithmus für OCD des Talus. Der gestrichelte Pfeil zeigt eine alternative Behandlung nach anfänglichem Misserfolg an. ACI = autologe Chondrozytenimplantation, CAM = kontrollierte Knöchelbewegung, CT = Computertomographie, H&P = Anamnese und körperliche Untersuchung, MACI = matrixunterstützte autologe Chondrozytenimplantation, MRT = Magnetresonanztomographie und OAT = osteochondrale Autotransplantation oder Allotransplantation [modifiziert nach 42]
Tibialis-posterior-Syndrom
Eine Dysfunktion von der Sehne des M. tibialis posterior ist der häufigste Grund für den erworbenen Plattfuß. Die Sehne des Musculus tibialis posterior ist überlastet, entzündet, degeneriert oder rupturiert. Dies kann zu einer schleichenden oder akuten Schwächung des Fußgewölbes führen [60].
Epidemiologie
Die Erkrankung tritt am häufigsten bei Frauen über 40 Jahren auf. Insgesamt betrifft das Syndrom mehr Frauen als Männer. Es ist eine der häufigsten Ursachen für einen erworbenen Plattfuß im Erwachsenenalter. Die Prävalenz nimmt mit zunehmendem Alter und bei bestimmten Risikofaktoren wie Adipositas oder rheumatischen Grunderkrankungen zu.
Pathogenese
Pathophysiologisch liegt dem Syndrom eine degenerative oder entzündliche Veränderung der Tibialis-posterior-Sehne zugrunde. Der Musculus tibialis posterior verläuft hinter dem Innenknöchel und ist für die Supination und Plantarflexion des Fußes sowie die Stabilisierung des medialen Längsgewölbes verantwortlich. Übermäßige oder chronische Belastung, degenerative Veränderungen oder systemische Erkrankungen (z. B. rheumatoide Arthritis) können zu einer Sehnenschädigung führen – von einer Tendinopathie bis hin zur Ruptur. Eine Insuffizienz der Sehne führt zu einer Fehlstellung (Valgusstellung) der Ferse, einem Absenken des Fußgewölbes und einer zunehmenden Fehlbelastung anderer Strukturen im Fuß [61].
Risikofaktoren
Risikofaktoren, die die Entstehung des Tibialis-posterior-Syndroms begünstigen, sind:
- Weibliches Geschlecht und höheres Alter
- Adipositas
- Überpronation des Fußes (Plattfußneigung)
- Diabetes mellitus
- Rheumatoide Arthritis
- Chronische Überlastung durch Sport oder langes Gehen/Stehen
- Vorangegangene Traumen im Bereich des Innenknöchels [62]
Symptome
Klinisch manifestiert sich das Tibialis-posterior-Syndrom initial durch belastungsabhängige Schmerzen entlang des medialen Sprunggelenks, insbesondere posterior des Malleolus medialis. Mit Fortschreiten der Erkrankung kommt es zu einer sichtbaren Abflachung des medialen Fußgewölbes und zu einer Valgisierung der Ferse. Charakteristisch ist die Unfähigkeit zum Einbein-Zehenstand auf der betroffenen Seite. Im fortgeschrittenen Stadium verlagert sich der Schmerz häufig auf den lateralen Fußrand infolge sekundärer Belastung des Sinus tarsi oder der Peronealsehnen.
Symptome des Tibialis–posterior-Syndroms
- Schmerz entlang des medialen Sprunggelenks oder im Bereich des Innenknöchels
- Schwellung an der Innenseite des Sprunggelenks
- Verlust des medialen Fußgewölbes (sichtbarer Plattfuß)
- Schwierigkeiten beim Einbein-Zehenstand
- Ermüdungsschmerz nach längerem Gehen
- Später häufig Verlagerung der Schmerzen auf den lateralen Fußrand durch sekundäre Belastungen
Therapie
Die Therapie richtet sich nach dem Stadium der Erkrankung.
Konservative Therapie
In frühen Stadien mit noch erhaltener Sehnenkontinuität steht die konservative Behandlung im Vordergrund. Diese umfasst eine Entlastung durch temporäre Immobilisierung, die Anwendung von nicht-steroidalen Antirheumatika (NSAR), physiotherapeutische Maßnahmen zur Kräftigung der Fußmuskulatur sowie die Versorgung mit individuell angepassten Einlagen oder Orthesen zur Unterstützung des medialen Fußgewölbes.
Konservative Therapie (bei Frühstadien)
- Stabilisierung mit Schiene oder Orthese [63]
- Physiotherapie zur Kräftigung der Fußmuskulatur [63, 64]
- Antientzündliche Maßnahmen (NSAR, Kühlen)
- Einlagenversorgung zur Unterstützung des medialen Fußgewölbes
- Reduktion belastender Aktivitäten [65]
- Ggf. Orthopädische Schuhversorgung
Operative Therapie
Bei fortgeschrittener Insuffizienz mit strukturellen Veränderungen und persistierenden Beschwerden ist eine operative Therapie indiziert [66]. Diese kann, je nach Befund, aus einem Sehnentransfer (z. B. Flexor-digitorum-longus-Sehne), knöchern-rekonstruktiven Maßnahmen wie einer medialisierenden Calcaneus-Osteotomie [67] oder bei ausgeprägter Deformität und Arthrose auch aus einer Arthrodese (Gelenkversteifung) bestehen. Ziel der chirurgischen Intervention ist die Wiederherstellung der Fußstatik und die Schmerzreduktion.
Posterior tibial tendon dysfunction
Die Posterior Tibial Tendon Dysfunction (PTTD) oder neuer als Konzept die Progressive Collapsing Foot Deformity (PCFD) beschreibt eine progrediente Funktionsinsuffizienz der Sehne des Musculus tibialis posterior, die zu einer zunehmenden Deformierung des Fußes mit Absenkung des medialen Längsgewölbes, Rückfuß-Valgus und Vorfuß-Abduktion führt [68]. Die Progression verläuft typischerweise über folgende Stadien [69]:
- Tendinose und Tenosynovitis mit struktureller Schwächung
- Elongation der Sehne und Verlust der dynamischen Gewölbestabilität
- Sekundäre ligamentäre Insuffizienz (Spring-Ligament, Deltoidband)
- Entwicklung einer fixierten Deformität mit arthrotischen Veränderungen im Subtalar- und oberen Sprunggelenk.
Die Johnson-und-Strom-Klassifikation ist klinisch weit verbreitet und differenziert vier Stadien [70]:
- Stadium I: Tendinopathie ohne strukturelle Deformität, Schwellung und Schmerzen, Einbein-Fersenstand möglich.
- Stadium II: Flexible Deformität mit abgesenktem Längsgewölbe, Rückfuß-Valgus und Vorfuß-Abduktion.
- Stadium III: Fixierte Deformität mit degenerativen Gelenkveränderungen.
- Stadium IV: Beteiligung des oberen Sprunggelenks mit Deltoidbandinsuffizienz und Sprunggelenksarthrose.
Diese Stadieneinteilung dient als Grundlage für die therapeutische Entscheidungsfindung [70]. Patienten mit einem Body-Mass-Index (BMI) über 30 erzielen bei rekonstruktiven Eingriffen schlechtere Ergebnisse als bei Rückfußfusionen. Gelenkerhaltende Verfahren sollten bei jungen Patienten versucht werden [71, 72].
Zusammenfassung
Bei den akuten Krankheitsbildern des Sprunggelenks handelt es sich meist um Sportverletzungen, die mit Frakturen im Bereich des oberen oder unteren Sprunggelenks und/oder Ruptur der gelenkstabilisierenden Bänder einhergehen. Die tatsächliche Prävalenz solcher Verletzungen ist aufgrund des sportartenabhängigen Verletzungsrisikos schwer zu erfassen. Schätzungsweise ist das Sprunggelenk jedoch in 30 bis 50 % aller Sportverletzungen involviert. Auch ein Knorpelschaden im oberen Sprunggelenk, Osteochondrosis dissecans oder ein Tibialis-posterior-Syndrom kommen als Ursache infrage.
Bei der Behandlung von Bandverletzungen des Sprunggelenks kommt meist ein konservatives Therapieschema zur Anwendung, das vergleichbare Ergebnisse liefert wie die operative Therapie. Eine Operation wird nur bei Läsionen des Schweregrades III in Erwägung gezogen.
Bei Frakturen ist die konservative Therapie bei nicht-dislozierten Verhältnissen möglich, ansonsten ist die anatomische Rekonstruktion z. B. mittels Osteosynthese durch einen operativen Eingriff notwendig.
Sowohl postoperativ als auch in der konventionellen Therapie von Bandrupturen spielen orthopädietechnische Hilfsmittel eine große Rolle, die in Abhängigkeit vom jeweils gewünschten Effekt ausgewählt werden.
Hinweis:
Aus Gründen der besseren Lesbarkeit wird auf die gleichzeitige Verwendung der Sprachformen männlich, weiblich und divers (m/w/d) verzichtet. Entsprechende Begriffe gelten im Sinne der Gleichbehandlung grundsätzlich für alle Geschlechter. Die verkürzte Sprachform beinhaltet keine Wertung.
Literatur
- Knupp M, Hintermann B (2006) Frakturen an Fuß und Sprunggelenk. In: Engelhardt M (Hrsg): Sportverletzungen. Diagnose, Management und Begleitmaßnahmen. Urban & Fischer Verlag, Elsevier GmbH, München, S. 291-297
- Menke W (2000) Spezielle Sportorthopädie und Sporttraumatologie. Limpert Verlag GmbH, Wiebelsheim, S. 101-124
- Menke W (2000) Kompendium der Sportverletzungen. Verlag im KILIAN, Marburg, S. 21-40
- Rammelt S, Grass R, Biewener A et al (2004) Anatomie, Biomechanik und Klassifikation der Sprunggelenkfrakturen. Trauma Berufskrankh 6 (Suppl 4): 384-392
- Wirth CJ (Hrsg) (2002) Orthopädie und orthopädische Chirurgie. Thieme Verlag, Stuttgart, S. 539
- S2e-Leitlinie Sprunggelenkfraktur. AWMF-Registernummer 012/003. Leitlinien der Deutschen Gesellschaft für Unfallchirurgie (DGU) im AWMF-Leitlinienprogramm. Verfügbar unter: . Stand 2015/2016
- AO-Foundation Education: Müllers AO Classification of Fractures – Long Bones. http://www.aofoundation.org/wps/portal/, AO Education, zuletzt am 20.10.2010
- Kapandji IA (1977) Funktionelle Anatomie der Gelenke. Schematisierte und kommentierte Zeichnungen zur menschlichen Biomechanik. Band 2: Untere Extremität. Enke Verlag, S. 150-191
- Mutschler W, Haas NP (Hrsg) (2007) Praxis der Unfallchirurgie. Thieme Verlag, Stuttgart, S. 534
- Schneiderbauer M, Valderrabano V (2006): Stressfrakturen des Unterschenkels und Fußes. In: Engelhardt M (Hrsg): Sportverletzungen. Diagnose, Management und Begleitmaßnahmen. Urban & Fischer Verlag, Elsevier GmbH, München, S. 297-302
- Grösele-Koppenburg A (2002) Stressfrakturen am Fuß und deren Behandlung. In: Engelhardt M, Freiwald J, Zichner L (Hrsg): Sprunggelenk und Fuß. Verletzungen und Überlastungsschäden. Novartis Pharma Verlag, Nürnberg, S. 131-149
- Zwipp, H (2023) Konservativ-funktionelle Behandlung der akuten fibularen Bandruptur des oberen Sprunggelenkes. Dtsch Arztebl Int 120: 454-60
- Buckkup K (2010) Klinische Tests an Knochen, Gelenken und Muskeln. Untersuchungen Zeichen Phänomene. Thieme Verlag, Stuttgart, S. 304-323
- Krüger-Franke M, Schurk B, Kugler A (2002) Diagnostik und Therapie der isolierten Ruptur der distalen tibiofibularen Syndesmose. In: Engelhardt M, Freiwald J, Zichner L (Hrsg): Sprunggelenk und Fuß. Verletzungen und Überlastungsschäden. Novartis Pharma Verlag, Nürnberg, S. 107-116
- Dubois B, Esculier J. (2020) Soft-tissue injuries simply need PEACE and LOVE. Br J Sports Med 54(2):72-73
- Kamin K et al (2025) Außenbandverletzungen am oberen Sprunggelenk. Unfallchirurgie 128: 47-58
- Zwipp, H (2023) Konservativ-funktionelle Behandlung der akuten fibularen Bandruptur des oberen Sprunggelenkes. Dtsch Arztebl Int 120: 454-460
- Lohrer H, Alt W, Gollhofer A, Rappe B (2000): Verletzungen am lateralen Kapselbandapparat des Sprunggelenks – eine Übersicht. Dtsch Z Sportmed 6: 196-203
- Petersen W (2009) Propriozeption, neuromuskuläre Kontrolle und funktionelle Stabilität. In: Petersen W, Zantop T (Hrsg): Das vordere Kreuzband. Grundlagen und aktuelle Praxis der operativen Therapie. Deutscher Ärzte-Verlag GmbH, Köln, S. 27
- Sell S, Zacher J, Lack S et al (1992) Kniegelenkspropriozeption bei der chronischen Polyarthritis. Akt Rheumatol 17: 173-177
- S1-Leitlinie Frische Außenbandruptur am Oberen Sprunggelenk, Deutsche Gesellschaft für Unfallchirurgie e.V. (DGU) in Zusammenarbeit mit der Österreichischen Gesellschaft für Unfallchirurgie (ÖGU), AWMF-Nr. 012-022, ICD S-93.40, S-93.41, S-93.42, S-93.43; letztes Bearbeitungsdatum: 08.08.2017, gültig bis 08.08.2022, Genehmigung durch Vorstand der DGU am 17.07.2017;
- Moreira V, Antuenes F (2008) Ankle sprain: from diagnosis to management. The physiatric view. Acta Med Port 21(3): 285-292
- Outerbridge RE (1961) The etiology of chondromalacia patellae. J Bone Joint Surg Br 43:752-757
- Outerbridge RE (1964) Further studies on the etiology of chondromalacia patellae. J Bone Joint Surg Br 46: 179-190
- Outerbridge RE, Dunlop JA (1975) The problem of chondromalacia patellae. Clin Orthop Relat Res 110: 177-196
- Mainil-Varlet P et al (2003) Histological assessment of cartilage repair: a report by the Histology Endpoint Committee of the International Cartilage Repair Society (ICRS). J Bone Joint Surg Am (85-A) Suppl 2: 45-57
- Harrasser N, von Eisenhart-Rothe R, Pohlig F et al (2017) Arthrose des oberen Sprunggelenks. Orthopäde 46: 625-638
- Buchhorn T, Weber J, Lampert C (2020) Arthrose des oberen Sprunggelenks. Arthroskopie 33: 1-3
- Bruns J, Habermann C, Werner M (2021) Osteochondral Lesions of the Talus: A Review on Talus Osteochondral Injuries, Including Osteochondritis Dissecans. Cartilage 13(Suppl 1) 1380S-1401S
- Jerosch J (2020) Konservative Therapie von Knorpelschäden am Sprunggelenk. Arthroskopie 33: 4-8
- Prado MP, Kennedy JG, Raduan F et al (2016) Diagnosis and treatment of osteochondral lesions of the ankle: current concepts. Rev Bras Ortop 51(5):489-500
- Shimozono Y, Yasui Y, Ross AW et al (2017) Osteochondral lesions of the talus in the athlete: up to date review. Curr Rev Musculoskelet Med 10:131-140
- Boffa A, Previtali D, Frattura GDL et al (2021). Evidence on ankle injections for osteochondral lesions and osteoarthritis: a systematic review and meta-analysis. Int Orthop 45(2):509-523
- Woo I, Park JJ, Seok HG (2023) The Efficacy of Platelet-Rich Plasma Augmentation in Microfracture Surgery Osteochondral Lesions of the Talus: A Systematic Review and Meta-Analysis. J Clin Med 12: 4998
- Cardoso RC, Andrade R, Monteiro I (2024) Operative Treatment of Nonprimary Osteochondral Lesions of the Talus: A Systematic Review. Orthop J Sports Med 12(12):23259671241296434
- Anwander H, Vetter P, Kurze C et al (2022) Evidence for operative treatment of talar osteochondral lesions: a systematic review. EFORT Open Rev 5;7(7):460-469
- Azam MT, Butler JJ, Duenes ML et al (2023) Advances in Cartilage Repair. Orthop Clin North Am 54(2):227-236
- Nguyen K, Cooperman S, Ng A (2024) Osteochondral Injuries of the Talus. Clin Podiatr Med Surg 41(3):437-450
- Grambart ST, Passet A, Holte N (2023) Osteochondral Lesions of the Talus: The Questions We Would Like Answered. Clin Podiatr Med Surg 40(3):425-437
- Qulaghassi M, Cho YS, Khwaja M et al (2021) Treatment strategies for osteochondral lesions of the talus: A review of the recent evidence. Foot (Edinb) 47:101805
- Tribe HC, McEwan J, Taylor H et al (2017) Mesenchymal Stem Cells: Potential Role in the Treatment of Osteochondral Lesions of the Ankle. Biotechnol J 12: 1700070
- Chau MM, Klimstra MA, Wise KL et al (2021) Osteochondritis Dissecans: Current Understanding of Epidemiology, Etiology, Management, and Outcomes. Bone Joint Surg Am 103(12): 1132-1151
- Tudisco C, Bernardi G, Manisera MT et al (2022) An update on osteochondritis dissecans of the knee. Orthop Rev 14: 38829
- Edmonds EW, Polousky J (2013) A Review of Knowledge in Osteochondritis Dissecans: 123 Years of Minimal Evolution from Ko¨nig to the ROCK Study Group. Clin Orthop Relat Res (2013) 471:1118-1126
- Bruns J (1997) Osteochondrosis dissecans: Diagnose und Therapie. In: Wirth CJ (ed.) Praxis der Orthopädie. Springer-Verlag
- Bruns J (1996) Osteochondrosis dissecans. Pathogenese, Diagnose und Therapie. Enke, Stuttgart
- International Cartilage Repair Society (ICRS). Cartilage lesion classification.
- Mainil-Varlet P, Aigner T, Brittberg M et al (2003) Histological assessment of cartilage repair: a report by the Histology Endpoint Committee of the International Cartilage Repair Society (ICRS). J Bone Joint Surg Am 85-A. Suppl 2:45-57
- Chambers HG, Shea KG, Carey JL (2011) AAOS Clinical Practice Guideline: Diagnosis and Treatment of Osteochondritis Dissecans. J Am Acad Orthop Surg 19(5): 307-309
- Mendeszoon MJ, Iosue HE (2022) Pediatric Osteochondritis Dissecans of the Talus. Clin Podiatr Med Surg 39(1):105-111
- Cabral J, Duart J (2023) Osteochondritis dissecans of the knee in adolescents: How to treat them? J Child Orthop 17(1):54-62
- Konarski W, Poboży T, Konarska K et al (2024) Understanding Osteochondritis Dissecans: A Narrative Review of the Disease Commonly Affecting Children and Adolescents. Children (Basel) 22;11(4):498
- Buda R, Pagliazzi G, Castagnini F et al (2016) Treatment of Osteochondritis Dissecans of the Talus in Skeletally Immature Population: A Critical Analysis of the Available Evidence. Foot Ankle Spec 9(3):265-70
- Pelletier-Roy R, Tran Y, Merle G (2024) Retroarticular drilling for osteochondritis dissecans of the talus: A systematic review. Orthop Traumatol Surg Res 110(7):103834
- Matthews JR, Sonnier JH, Paul RW et al (2023) A systematic review of cartilage procedures for unstable osteochondritis dissecans. Phys Sportsmed 51(6):497-505
- Aurich M, Albrecht D, Angele P et al (2017) Treatment of Osteochondral Lesions in the Ankle: A Guideline from the Group „Clinical Tissue Regeneration“ of the German Society of Orthopaedics and Traumatology (DGOU). Z Orthop Unfall 155(1):92-99
- Chambers HG, Shea KG, Carey JL et al (2011) AAOS Clinical Practice Guideline: diagnosis and treatment of osteochondritis dissecans. J Am Acad Orthop Surg 19(5):307-9
- American Academy of Orthopaedic Surgeons (AAOS). Clinical practice guidelines on the diagnosis and treatment of osteochondritis dissecans. https://www.aaos.org
- The Diagnosis and Treatment of Osteochondritis Dissecans Evidence-Based Clinical Practice Guideline Adopted by: The American Academy of Orthopaedic Surgeons Board of Directors December 4, 2010.
- Bubra PS, Keighley G, Rateesh S et al (2015) Posterior Tibial Tendon Dysfunction: An Overlooked Cause of Foot Deformity. J Family Med Prim Care 4(1): 26-29
- Ling SKK, Lui TH (2017) Posterior Tibial Tendon Dysfunction: An Overview. Open Orthop J 11:714-723
- Knapp PW, Constant D (2024) Posterior Tibial Tendon Dysfunction. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan
- Gómez-Jurado I, Juárez-Jiménez JM and Munuera-Martínez PV (2021) Orthotic treatment for stage I and II posterior tibial tendon dysfunction (flat foot): A systematic review. Clinical Rehabilitation 35(2): 159-168
- Ross MH, Smith MD, Mellor R (2018) Exercise for posterior tibial tendon dysfunction: a systematic review of randomised clinical trials and clinical guidelines. BMJ Open Sport Exerc Med 4:e000430
- Rhim HC, Dhawan R, Gureck AE et al (2022) Characteristics and Future Direction of Tibialis Posterior Tendinopathy Research: A Scoping Review. Medicina (Kaunas) 58(12):1858
- Piraino JA, Theodoulou MH, Ortiz J et al (2020) American College of Foot and Ankle Surgeons Clinical Consensus Statement: Appropriate Clinical Management of Adult-Acquired Flatfoot Deformity. J Foot Ankle Surg 59(2):347-355
- Manway JM (2023) Single and Double Osteotomies of the Calcaneus for the Treatment of Posterior Tibial Tendon Dysfunction. Clin Podiatr Med Surg 40(2):261-269
- Knapp PW, Constant D. (2024) Posterior Tibial Tendon Dysfunction. [Updated 2024 May 21]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. Available from:
- Ling SKK, Lui TH (2017) Posterior tibial tendon dysfunction: An overview. Open Orthop J 11: 714-720
- Johnson KA, Strom DE (1989) Tibialis posterior tendon dysfunction. Clin Orthop Relat Res 239: 196-206
- Myerson MS, Thordarson DB, Johnson JE et al (2020) Classification and Nomenclature: Progressive Collapsing Foot Deformity. Foot Ankle Int 41(10):1271-1276
- Sangeorzan BJ, Hintermann B, de Cesar Netto C et al (2020) Progressive Collapsing Foot Deformity: Consensus on Goals for Operative Correction. Foot Ankle Int 41(10):1299-1302




Tutorielle Unterstützung
Die tutorielle Unterstützung der Fortbildungsteilnehmer erfolgt durch unseren ärztlichen Leiter Dr. med. Alexander Voigt in Zusammenarbeit mit der arztCME-Redaktion. Inhaltliche Fragen können über das Kommentarfeld, direkt per Mail an service@arztcme.de oder via Telefon unter Tel.: +49(0)180-3000759 gestellt werden. Inhaltliche Fragen werden von unserem ärztlichen Leiter bzw. nach Rücksprache mit diesem und evtl. dem Autor auch von der arztCME-Redaktion beantwortet.
Technischer Support
Der technische Support der Online-Akademie arztCME.de erfolgt durch geschulte Mitarbeiterinnen und Mitarbeiter des Betreibers health&media GmbH unter der E-Mail-Adresse technik@arztcme.de oder via Telefon unter Tel.: 49(0)180-3000759.