Sequenztherapie der Osteoporose mit Fokus auf Teriparatid und Denosumab
Interessengebiete: Allgemeinmedizin und Innere Medizin, Orthopädie, Geriatrie
Osteoporose ist eine chronische Erkrankung, die mit einem erhöhten Risiko für Knochenbrüche, im Alter einhergeht. Moderne Therapiekonzepte gehen über die reine Erhöhung der Knochendichte hinaus und fokussieren auf die nachhaltige Frakturprävention durch individuell angepasste Therapiesequenzen. In diesem Kurs werden die Wirkmechanismen und der klinische Einsatz von Teriparatid (osteoanabol) und Denosumab (antiresorptiv) erläutert, die Rolle einer sinnvollen Abfolge der Behandlungsschritte diskutiert und praxisrelevante Empfehlungen für die individuell abgestimmte Anwendung gegeben.
Kursinhalt
Inhaltsverzeichnis
- Einleitung
- Therapeutisches Ziel: Frakturprävention
- Pharmakologische Grundlagen der Osteoporosetherapie
- Warum die Therapiesequenz entscheidend ist
- Risikostratifikation und Leitlinienempfehlungen
- Exit-Strategien
- Evidenzbasierte Betrachtung von Teriparatid
- Evidenzbasierte Betrachtung von Denosumab
- Sequenzstrategien mit Fokus Teriparatid und Denosumab
- Versorgungsumsetzung
- Fazit
- Literatur
Einleitung
Die Osteoporose ist eine chronische, systemische Skeletterkrankung, die durch eine reduzierte Knochenfestigkeit und ein daraus resultierendes erhöhtes Frakturrisiko gekennzeichnet ist. Osteoporotische Frakturen – insbesondere Wirbelkörper-, Hüft- und proximale Humerusfrakturen – stellen eine der häufigsten Ursachen für Morbidität, funktionellen Verlust und Mortalität im höheren Lebensalter dar und sind mit erheblichen sozioökonomischen Belastungen verbunden [1].
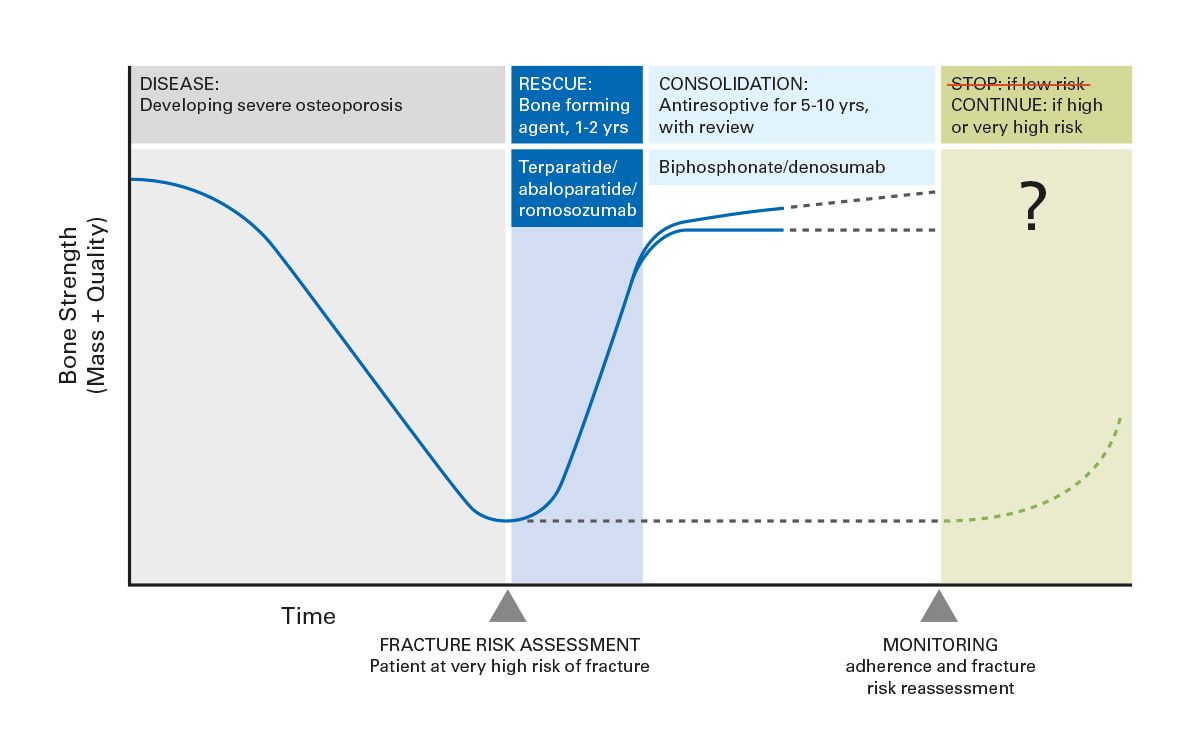
Trotz der Verfügbarkeit wirksamer medikamentöser Therapien zur Verminderung des Frakturrisikos wird dadurch die Osteoporose nicht geheilt und das Frakturrisiko ist bei den Patient*innen dauerhaft erhöht. Während die Osteoporose früher regelmäßig als statische Erkrankung gesehen wurde mit eine Frakturrisiko aufgrund einer niedrigen Knochendichte, wird zunehmend bewusst, dass es sich vielmehr um einen dynamischen Prozess mit altersabhängiger Progression, wechselnden Risikokonstellationen und damit zeitlich variierender erforderlicher Therapieantwort handelt [2, 3]. Vor diesem Hintergrund haben in den letzten Jahren Überlegungen zur Sequenztherapie als zentralem Bestandteil eines modernen Osteoporosemanagements vermehrt Aufmerksamkeit erfahren (Abb. 1).
Die Sequenztherapie berücksichtigt, dass antiresorptive und osteoanabole Substanzen grundlegend unterschiedliche Wirkmechanismen auf den Knochenstoffwechsel, die Mikroarchitektur und die Materialeigenschaften des Knochens ausüben. Diese Unterschiede haben nicht nur unmittelbare Konsequenzen für die kurzfristige Frakturreduktion, sondern beeinflussen auch maßgeblich die Wirksamkeit nachfolgender Therapien [4, 5]. Insbesondere die Wahl der Ersttherapie spielt eine entscheidende Rolle für den langfristigen Behandlungserfolg.
Teriparatid als Vertreter der osteoanabolen Therapie mit remodeling-basierter Knochenneubildung und Denosumab als hochpotentes antiresorptives Medikament mit rascher und ausgeprägter Hemmung des Knochenabbaus nehmen hierbei eine besondere Stellung ein. Beide Substanzen zeigen eine frühe und signifikante Reduktion des Frakturrisikos, unterscheiden sich jedoch deutlich hinsichtlich ihrer biologischen Effekte, ihrem Stellenwert in der Langzeitstrategie und den Anforderungen an eine sichere Beendigung bzw. Umstellung der Therapie [6, 7].
Aktuelle nationale und internationale Leitlinien, darunter die DVO-Leitlinie 2023 [8], tragen dieser Entwicklung Rechnung, indem sie eine risikoadaptierte, individualisierte Therapieplanung fordern und bei Patient*innen mit hohem oder imminentem Frakturrisiko explizit den frühzeitigen Einsatz osteoanabol wirksamer Substanzen ermöglichen oder empfehlen (Abb. 2). Für die klinische Praxis ergibt sich daraus die Notwendigkeit, Therapieentscheidungen nicht isoliert, sondern im Kontext einer vorausschauenden, langfristigen Sequenz zu treffen.
Dieser CME-Beitrag soll Hausärzt*innen sowie relevanten Fachärzt*innen eine evidenzbasierte, praxisnahe Orientierung zur Sequenztherapie der Osteoporose geben, mit besonderem Fokus auf Teriparatid und Denosumab.
Therapeutisches Ziel: Frakturprävention
Das primäre Ziel jeder Osteoporosetherapie ist die nachhaltige Reduktion des Frakturrisikos. Frakturen stellen das klinisch relevante Endereignis der Erkrankung dar und sind mit erhöhter Mortalität, funktionellen Einschränkungen, Pflegebedürftigkeit und einer signifikanten Reduktion der Lebensqualität assoziiert [1]. Die therapeutische Zielgröße geht dabei über eine reine Zunahme der Knochendichte (Bone Mineral Density, BMD) hinaus.
Die Knochenfestigkeit wird durch mehrere Komponenten bestimmt, darunter die Knochenmasse, die Mikroarchitektur (trabekuläre Konnektivität, kortikale Dicke und Porosität), die Materialeigenschaften der Knochenmatrix sowie die geometrische Struktur des Knochens [2]. Veränderungen dieser Parameter können in gewissen Ausmaß unabhängig voneinander auftreten und sind nur teilweise durch die DXA-basierte Knochendichtemessung abbildbar.
Antiresorptive Therapien führen primär zu einer Reduktion des Knochenumbaus und zu einer verstärkten sekundären Mineralisation, wodurch sich die gemessene Knochendichte erhöht. Osteoanabole Therapien hingegen verbessern die Knochenqualität durch strukturelle Neubildung und Reorganisation des Knochens [4]. Diese unterschiedlichen biologischen Effekte haben direkte Konsequenzen für die Frakturreduktion und für die langfristige Stabilität des Skeletts.
Ein modernes Osteoporosemanagement muss daher die Verbesserung der Knochenresilienz als integratives Therapieziel verfolgen und die Wahl sowie Abfolge medikamentöser Interventionen an diesem Ziel ausrichten.
Pharmakologische Grundlagen der Osteoporosetherapie
Antiresorptive Therapieprinzipien
Antiresorptive Substanzen hemmen den Knochenabbau durch Inhibition der Osteoklastenaktivität. Zu dieser Substanzklasse gehören insbesondere Bisphosphonate und Denosumab.
Denosumab ist ein monoklonaler Antikörper gegen den RANK-Liganden und blockiert die Differenzierung, Aktivierung und das Überleben von Osteoklasten. Die Folge ist eine rasche und ausgeprägte Reduktion des Knochenumbaus in allen Skelettkompartimenten [5]. Durch die verminderte Resorption kommt es zu einer verstärkten sekundären Mineralisation, zur Reduktion der kortikalen Porosität und zu einer Zunahme der BMD.
Die antiresorptive Wirkung ist vollständig reversibel und an die kontinuierliche Gabe gebunden. Nach Absetzen kommt es zu einem überschießenden Wiederanstieg des Knochenumbaus mit potenziell relevantem Frakturrisiko, was für die Therapieplanung von zentraler Bedeutung ist [6].
Osteoanabole Therapieprinzipien
Teriparatid ist ein rekombinantes Parathormonfragment (PTH 1–34), das bei intermittierender Gabe eine osteoanabole Wirkung entfaltet. Der Wirkmechanismus beruht primär auf einer remodeling-basierten Knochenneubildung, bei der zunächst alter, mikrostrukturell geschädigter Knochen resorbiert und anschließend durch neu gebildeten, qualitativ hochwertigen Knochen ersetzt wird [7].
Dieser Prozess geht initial mit einer Aktivierung des Knochenumbaus einher und kann insbesondere an kortikalen Strukturen zu einer vorübergehenden Abnahme der gemessenen Knochendichte führen. Diese densitometrische Veränderung spiegelt jedoch keine Verschlechterung der Knochenstabilität wider, sondern ist Ausdruck der verzögerten sekundären Mineralisation des neu gebildeten Knochens.
Langfristig führt Teriparatid zu einer Verbesserung der trabekulären Konnektivität, zu periostalem Knochenaufbau und zu einer strukturellen Stärkung des Skeletts.
Warum die Therapiesequenz entscheidend ist
Die Wirkung einer Osteoporosetherapie ist nicht isoliert zu betrachten, sondern beeinflusst maßgeblich die Wirksamkeit nachfolgender Behandlungen. Dieses Konzept der Therapiesequenz ist insbesondere im Kontext der osteoanabolen Therapie von zentraler Bedeutung.
Eine vorausgegangene intensive antiresorptive Therapie kann den Knochenstoffwechsel so stark dämpfen, dass die anabole Antwort auf Teriparatid abgeschwächt ist. Umgekehrt lässt sich eine durch osteoanabole Therapie aufgebaute Knochenstruktur durch anschließende antiresorptive Behandlung effektiv konsolidieren [3].
Bei Patient*innen mit sehr hohem oder imminentem Frakturrisiko kann ein primär osteoanaboler Therapieansatz zu einer rascheren und nachhaltigeren Risikoreduktion führen als eine sequenzielle Eskalation nach Frakturereignissen.
Risikostratifikation und Leitlinienempfehlungen
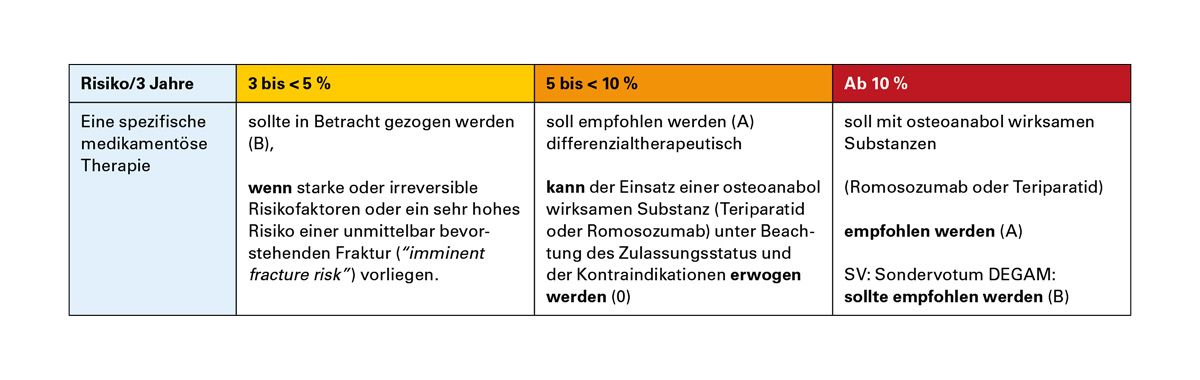
Die DVO-Leitlinie 2023 empfiehlt eine individuelle Risikostratifikation anhand des 3-Jahres-Frakturrisikos für Wirbelkörper- und Hüftfrakturen [8]. Bereits ab einem Risiko von ≥ 3 % kann eine spezifische medikamentöse Therapie erwogen werden, während ab ≥ 5 % eine klare Therapieempfehlung besteht.
Bei einem 3-Jahres-Risiko von ≥ 10 % oder bei Vorliegen eines hohen imminenten Frakturrisikos wird der bevorzugte Einsatz osteoanabol wirksamer Substanzen empfohlen, sofern keine Kontraindikationen bestehen.
Ein imminentes Frakturrisiko liegt insbesondere bei frischen Wirbelkörper- oder Hüftfrakturen, multiplen Frakturen innerhalb kurzer Zeit, häufigen Stürzen oder neu begonnener systemischer Glukokortikoidtherapie vor [9]. In dieser Situation ist eine rasch wirksame Therapie mit früher Frakturreduktion erforderlich. Sowohl Teriparatid als auch Denosumab zeigen eine signifikante Wirksamkeit innerhalb der ersten 12 Monate und sind daher für diese Hochrisikokonstellationen besonders relevant [10].
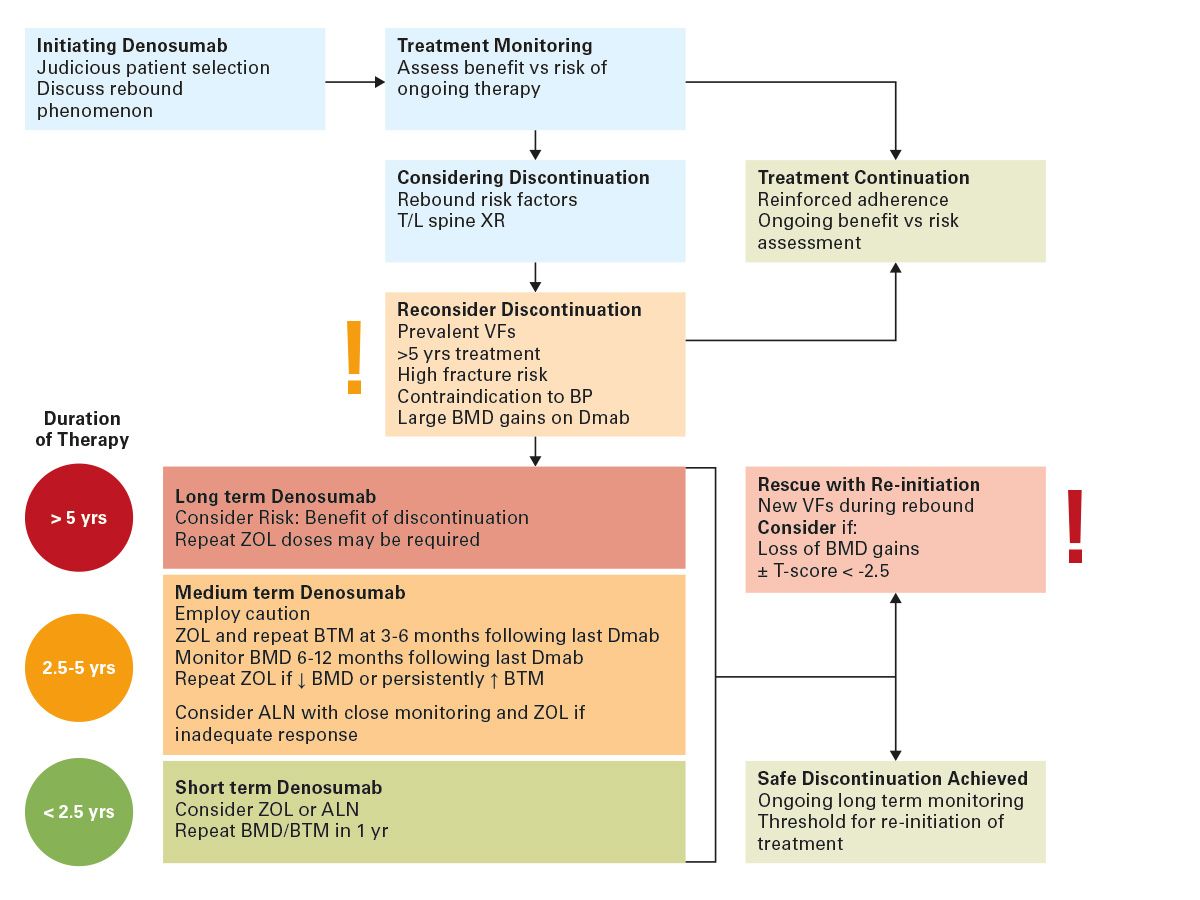
Exit-Strategien
Internationale Positionspapiere und systematische Reviews empfehlen nach Absetzen von Denosumab eine zeitgerechte antiresorptive Anschlussbehandlung, um den Rebound-Knochenumsatz zu dämpfen und BMD-Verluste / Frakturen zu verhindern. [11, 12].
Randomisierte Daten zeigen, dass Zoledronat nach Denosumab BMD-Verluste reduziert. Der Effekt kann jedoch interindividuell variieren und ist u. a. vom Denosumab-Vorbehandlungszeitraum und vom Zeitpunkt der Zoledronatgabe abhängig [8]. Orale Bisphosphonate (z. B. Alendronat) können eine Alternative darstellen, v. a. wenn i. v. Therapie nicht möglich ist und die vorherige Denosumabbehandlung nur über einen begrenzenten Zeitraum von wenigen Jahren erfolgte. Die Wirksamkeit zur vollständigen Rebound-Prävention ist heterogen und hängt wesentlich von der Dauer der vorherigen Denosumab-Therapie sowie natürlich der Adhärenz zur Anschlusstherapie sowie von der Resorption des jeweiligen Präparates ab [11, 12].
Nach osteoanaboler Therapie (z. B. Teriparatid) ist Denosumab eine valide Konsolidierungsoption, um anabole Gewinne zu stabilisieren und weiter auszubauen. Bei einem Wechsel von Denosumab zu Teriparatid sollte man sich bewusst sein, dass es zu einem transientem BMD-Verlust (insbesondere an Hüfte/Radius) kommen kann. Erfreulicher Weise haben die entsprechenden Studien kein erhöhtes Frakturrisiko in diesem Zusammenhang gezeigt. Dennoch sollte dieser Pfad nur bei klarer Indikation mit einem explizitem Managementplan und im Bewusstsein um diese Tatsache erfolgen [13].
Evidenzbasierte Betrachtung von Teriparatid
Teriparatid (rhPTH 1-34) ist ein osteoanaboles Therapeutikum. Bei intermittierender Gabe stimuliert es osteoblastäre Aktivität und Knochenformation, verbessert Mikroarchitekturparameter und führt zu raschem BMD-Anstieg v. a. an der Wirbelsäule. Teriparatid ist insbesondere für Patient*innen mit sehr hohem Frakturrisiko und / oder multiplen Frakturen bzw. hohem kurzfristigem Risiko relevant, wenn ein schneller, strukturverbessernder Therapieeffekt klinisch prioritär ist [5, 9, 10].
In der pivotalen NEJM-Studie reduzierte Teriparatid (20 µg täglich s. c.) signifikant das Risiko vertebraler und nicht-vertebraler Frakturen bei postmenopausaler Osteoporose [14].
Ein wesentlicher Punkt für die Versorgung ist, dass osteoanabole Therapien in Metaanalysen / Netzwerkvergleichen als besonders geeignet für Patient*innen mit hohem kurzfristigem Risiko diskutiert werden, weil sie rasch wirksame Effekte auf vertebrale Endpunkte zeigen [10].
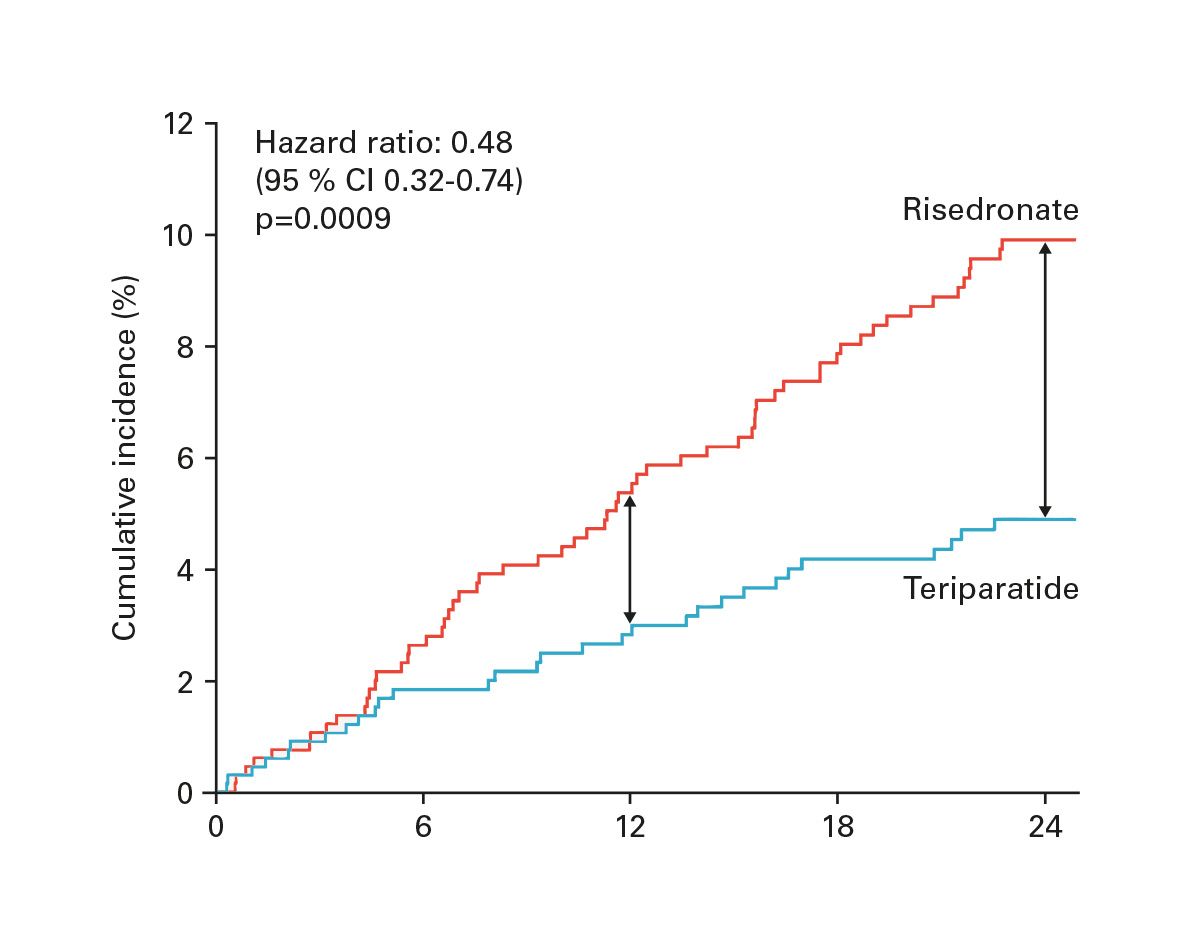
In der VERO-Studie reduzierte Teriparatid bei Patient*innen mit schwerer Osteoporose das Risiko für neue Wirbelkörperfrakturen im Vergleich zu Risedronat um etwa 50 % [15]. Der Effekt nahm mit zunehmender Therapiedauer zu und spiegelte die progressive strukturelle Verbesserung des Knochens wider (Abb. 3).
Teriparatid wird zeitlich begrenzt eingesetzt (gemäß EMA-Zulassung bis zu 24 Monate einmal im Leben). Übelkeit, Schwindel, Beinkrämpfe sowie initiale Hyperkalzämien sind möglich, weshalb Kalziumzufuhr und Laborkontrollen in der Startphase individuell zu planen sind.
Die osteoanabole Wirksamkeit von Teriparatid ist bei therapienaiven Patient*innen am stärksten ausgeprägt. Nach Vorbehandlung mit hochaffinen Bisphosphonaten ist der densitometrische Anstieg verzögert und abgeschwächt, während die Frakturreduktion dennoch früh einsetzt [10, 16]. Teriparatid zeigt eine besondere Überlegenheit bei der glukokortikoidinduzierten Osteoporose sowie bei Männern mit Osteoporose [17,18].
Nach Absetzen von Teriparatid kann es ohne Anschlussbehandlung zu einem Rückgang der BMD kommen. Daher ist nach Abschluss der anabolen Phase eine antiresorptive Konsolidierung Standard, um die strukturellen und densitometrischen Gewinne zu erhalten. Denosumab ist hierfür eine potente Option – auch Bisphosphonate sind etablierte Konsolidierungsstrategien [10,13].
Evidenzbasierte Betrachtung von Denosumab
Der Wechsel von Bisphosphonaten zu Denosumab ist mit einem zusätzlichen Zugewinn an Knochendichte assoziiert und stellt eine effektive Sequenzoption dar, insbesondere bei unzureichender Wirksamkeit oder eingeschränkter Adhärenz unter oralen Bisphosphonaten [17].
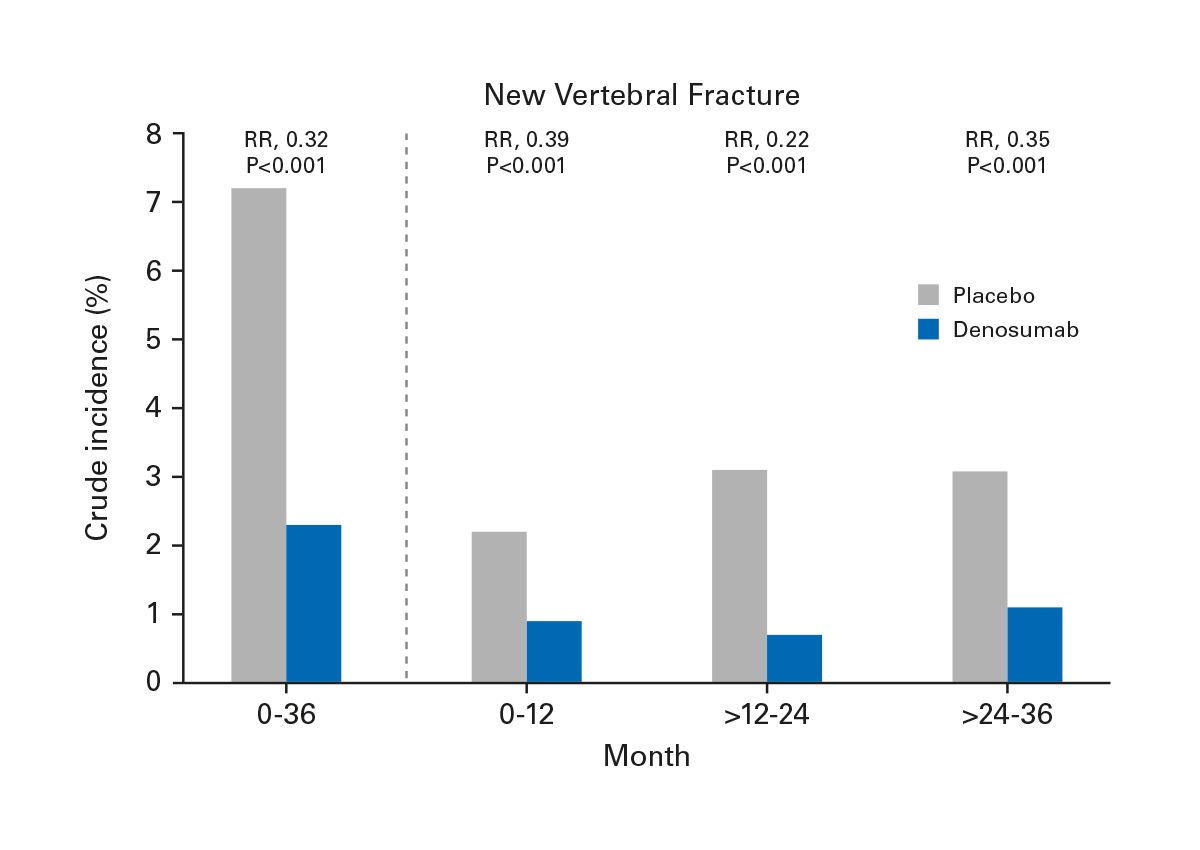
In der randomisierten, placebokontrollierten FREEDOM-Studie reduzierte Denosumab über 36 Monate signifikant das Risiko neuer vertebraler Frakturen, nicht-vertebraler Frakturen und Hüftfrakturen bei postmenopausaler Osteoporose [18] (Abb. 4). Die offene Verlängerungsphase bis zu 10 Jahre (FREEDOM Extension) zeigte anhaltend niedrige Frakturraten bei fortgesetzter Therapie sowie progressive BMD-Zunahmen ohne erkennbares Plateau [19]. Diese Langzeitdaten stützen die Rolle von Denosumab als wirksame Option bei Patient*innen mit dauerhaft hohem Frakturrisiko.
Unter Denosumab sind die in der Osteoporosetherapie relevanten seltenen unerwünschten Ereignisse (insbesondere Kieferosteonekrose, ONJ und atypische Femurfrakturen, AFF) insgesamt selten, müssen aber in die Nutzen-Risiko-Abwägung und in das Monitoring einbezogen werden [19]. Vor Beginn sollten relevante dentale Risikofaktoren erhoben und – wenn möglich – invasive Eingriffe vor Therapiebeginn abgeschlossen werden. Unter Therapie sind stringente Mundhygiene und regelhafte zahnärztliche Kontrollen sinnvoll. Ausreichende Versorgung mit Kalzium/Vitamin D ist obligat.
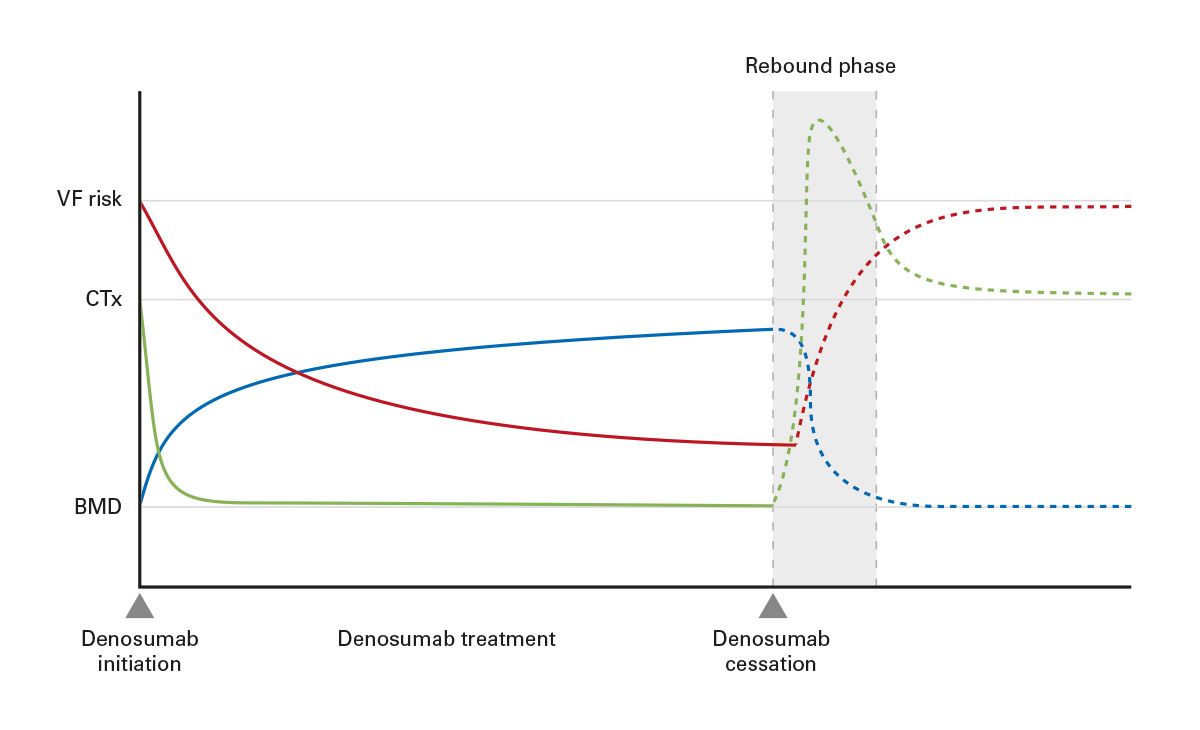
Im Gegensatz zu Bisphosphonaten besitzt Denosumab keine knochenbindende Depotwirkung. Nach Absetzen kommt es – zeitlich korreliert mit dem Auslaufen der pharmakologischen Wirkung – zu einem raschen Anstieg der Knochenumbaumarker, zu beschleunigtem BMD-Verlust und bei einem Teil der Patient*innen zu multiplen klinisch manifesten Wirbelkörperfrakturen (rebound-associated vertebral fractures) [20]. Denosumab sollte nicht ohne geplante Anschlussstrategie beendet werden.
Das Absetzen von Denosumab ohne anschließende antiresorptive Therapie ist mit einem raschen Anstieg des Knochenumbaus und einem erhöhten Risiko für multiple Wirbelkörperfrakturen verbunden [21] (Abb. 5). Eine strukturierte Anschlusstherapie, meist mit einem Bisphosphonat, ist obligat und sollte anhand von Knochenumbaumarkern überwacht werden (Abb. 6).
Sequenzstrategien mit Fokus Teriparatid und Denosumab
Während Denosumab primär durch Reduktion des Knochenabbaus wirkt, induziert Teriparatid eine strukturelle Neubildung des Knochens. Beide Strategien führen über unterschiedliche biologische Wege zu einer effektiven Frakturreduktion [7, 8]. Diese komplementären Effekte bilden die Grundlage für rationale Sequenztherapien, bei denen ein osteoanaboler Aufbau durch eine antiresorptive Konsolidierung stabilisiert wird.
Die DATA-Switch-Studie untersuchte den Übergang zwischen Teriparatid und Denosumab. Zentrale klinische Implikation:
- Teriparatid → Denosumab: weiterer BMD-Anstieg an allen Messorten
- Denosumab → Teriparatid: transienter BMD-Abfall an Hüfte / Wirbelsäule und progressiver Verlust am distalen Radius
Diese Ergebnisse sind unmittelbar sequenzrelevant und sprechen dafür, bei Denosumab-Vorbehandlung eine sehr sorgfältige Indikationsstellung und ein explizites Managementkonzept für einen Wechsel zu Teriparatid zu verlangen [13].
Wichtig ist auch zu wissen, dass es nicht allein um die Knochendichte geht, sondern auch um die Biologie des Knochens. Anhand von erfundenen Patient*innen lassen sich mögliche Sequenzen einer Behandlung simulieren. Dazu gehören folgende Überlegungen:
- Mit welchem Präparat soll gestartet werden?
- Wie viele Jahre soll behandelt werden?
- Was wird die nächste und übernächste Therapie sein?
Dadurch, dass diese Präparate jetzt auch als Biosimilars zur Verfügung stehen, kann die Therapie sowohl mit Teriparatid als auch mit Denosumab wirtschaftlich umgesetzt werden.
Versorgungsumsetzung
Primärziel ist die Reduktion klinisch relevanter Fragilitätsfrakturen. BMD-Veränderungen sind ein Surrogat, dessen Interpretation immer im Kontext von Ausgangsrisiko, Frakturereignissen, Adhärenz und Therapiedauer erfolgen muss. Leitlinien empfehlen eine strukturierte Verlaufskontrolle und Anpassung bei Ereignissen unter Therapie [8]. Als Basisdiagnostik vor Therapie und bei Wechsel gelten für beide Substanzen:
- Anamnese: Frakturen, Stürze, Glukokortikoide, CKD, Malabsorption, Tumoranamnese, zahnmedizinische Risiken
- Labore: Calcium, Phosphat, Kreatinin / eGFR, 25-OH-Vitamin D, ggf. PTH (Differenzialdiagnosen), TSH je nach Kontext
- DXA (LWS / Hüfte) + Wirbelkörperstatus (VFA / Röntgen) bei Verdacht auf asymptomatische Wirbelfrakturen [8]
Zusätzlich vor Denosumab-Gabe Hypokalzämierisiko aktiv abklären und korrigieren sowie Vitamin-D-Mangel behandeln. Vor Teriparatid sollte eine Hyperkalzämie ausgeschlossen werden.
Die Hausarztrolle umfasst in diesem Konzept Risikoidentifikation (Indexfraktur, Sturzrisiko, Glukokortikoide), Basisdiagnostik, Termin-/Adhärenzmanagement, Koordination DXA / Wirbelstatus, Vitamin-D-/Calcium-Optimierung. Zur fachärztlichen Rolle (Endokrinologie / Rheumatologie / Orthopädie / Gynäkologie) gehören die Indikationsstellung bei sehr hohem Risiko, Sequenzentscheidungen sowie das Management komplexer Komorbiditäten.
Fazit
Die Osteoporose ist eine chronische, systemische Skeletterkrankung, die durch abnehmende Knochenfestigkeit und ein erhöhtes Frakturrisiko charakterisiert ist. Insbesondere Wirbelkörper-, Hüft- und proximale Humerusfrakturen stellen die häufigsten Ursachen für Morbidität, funktionellen Verlust und Mortalität bei älteren Menschen dar und belasten das Gesundheitssystem erheblich.
Eine evidenzbasierte Behandlung verfolgt den Ansatz eines risikoadaptierten Therapieplans: Die Auswahl von Medikamenten erfolgt je nach Fragilität, Frakturtyp, Knochenmineraldichte (BMD) und individuellen Risikofaktoren. Ein leitliniengerechtes Vorgehen bei hohem Frakturrisiko basiert auf einer individuellen medikamentösen Therapie, die sowohl die Häufigkeit von Wiederholungsfrakturen reduziert als auch Nebenwirkungen minimiert.
Für die klinische Praxis bedeutet dies: Frühe Risiko-Assessment-Tools, konsequente BMD-Messungen, individualisierte Medikamentenwahl und regelmäßige Therapie-Überwachung, um die Osteoporose-Komplikationen effektiv zu verringern.
Literatur
- Compston J et al. Osteoporosis. Lancet 2019; 393: 364-376
- Seeman E, Delmas PD. Bone Quality — The Material and Structural Basis of Bone Strength and Fragility.N Engl J Med 2006; 354: 2250-2261
- Curtis JR et al. Management of patients at very high risk of osteoporotic fractures through sequential treatments. Aging Clin Exp Res 2022; 34: 695–714
- Choksi P et al. The challenges of diagnosing osteoporosis and the limitations of currently available tools. Clin Diabetes Endocrinol 2018: 4: 12
- Cummings SR et al. Denosumab for Prevention of Fractures in Postmenopausal Women with Osteoporosis. N Engl J Med 2009; 361: 756-765
- Miller PD et al. Effect of denosumab on bone density and turnover in postmenopausal women with low bone mass after long-term continued, discontinued, and restarting of therapy: a randomized blinded phase 2 clinical trial.Bone 2008; 43: 222-229
- Dempster DW et al. Remodeling- and Modeling-Based Bone Formation With Teriparatide Versus Denosumab: A Longitudinal Analysis From Baseline to 3 Months in the AVA Study. J Bone Miner Res 2018; 33: 298-306
- DVO-Leitlinie Prophylaxe, Diagnostik und Therapie der Osteoporose bei postmenopausalen Frauen und bei Männern ab dem 50. Lebensjahr (S3-Leitlinie, AWMF-Register-Nr. 183-001
- Kanis JA et al. Algorithm for the management of patients at low, high and very high risk of osteoporotic fractures. Osteoporos Int 2020; 31: 1-12
- Laura M et al. Which treatment to prevent an imminent fracture? Bone Rep 2021; 15: 101105
- Tsourdi E et al. Fracture risk and management of discontinuation of denosumab therapy: a systematic review and position statement by ECTS. J Clin Endocrinol Metab 2021; 106: 264–281
- Bone HG et al. Effects of denosumab treatment and discontinuation on bone mineral density and bone turnover markers in postmenopausal women with low bone mass. J Clin Endocrinol Metab.2011; 96: 972–980
- Leder BZ et al. Denosumab and teriparatide transitions in postmenopausal osteoporosis (the DATA-Switch study): extension of a randomised controlled trial. Lancet 2015;386: 1147–1155
- Neer RM et al. Effect of parathyroid hormone (1-34) on fractures and bone mineral density in postmenopausal women with osteoporosis. N Engl J Med 2001; 344: 1434–1441
- Kendler DL et al. Effects of teriparatide and risedronate on new fractures in post-menopausal women with severe osteoporosis (VERO): a multicentre, double-blind, double-dummy, randomised controlled trial. Lancet 2018; 391: 230-240
- Lindsay R et al. Teriparatide for osteoporosis: importance of the full course. Osteoporos Int 2016; 27: 2395-410
- Miller PD et al. Efficacy and safety of denosumab vs. bisphosphonates in postmenopausal women previously treated with oral bisphosphonates. Osteoporos Int 2020 ; 31 : 181-191
- Cummings SR, San Martin J, McClung MR, et al. Denosumab for prevention of fractures in postmenopausal women with osteoporosis. N Engl J Med 2009; 361: 756–765
- Bone HG et al. 10 years of denosumab treatment in postmenopausal women with osteoporosis: results from the phase 3 randomised FREEDOM trial and open-label extension. Lancet Diabetes Endocrinol 2017; 5: 513–523
- Anastasilakis AD et al. Denosumab discontinuation and the rebound phenomenon: a narrative review. J Clin Med 2021; 10: 152
- Kumar S et al. Denosumab discontinuation in the clinic – implications of rebound bone turnover and emerging strategies to prevent bone loss and fractures. J Bone Miner Res 2025; 40: 1017-1034

Tutorielle Unterstützung
Die tutorielle Unterstützung der Fortbildungsteilnehmer erfolgt durch unseren ärztlichen Leiter Dr. med. Alexander Voigt in Zusammenarbeit mit der arztCME-Redaktion. Inhaltliche Fragen können über das Kommentarfeld, direkt per Mail an service@arztcme.de oder via Telefon unter Tel.: +49(0)180-3000759 gestellt werden. Inhaltliche Fragen werden von unserem ärztlichen Leiter bzw. nach Rücksprache mit diesem und evtl. dem Autor auch von der arztCME-Redaktion beantwortet.
Technischer Support
Der technische Support der Online-Akademie arztCME.de erfolgt durch geschulte Mitarbeiterinnen und Mitarbeiter des Betreibers health&media GmbH unter der E-Mail-Adresse technik@arztcme.de oder via Telefon unter Tel.: 49(0)180-3000759.